в московской школе
Синтез аденинового мономера пептидно-нуклеиновых кислот на основе L-глутаминовой кислоты с циклогексильной защитой и оценки его выхода
|
Работа призёра открытой городской научно-практической конференции «Инженеры будущего» в секции «IT в медицине, биомедицинские технологии, медицинское приборостроение, бионика» среди работ учащихся 10−11 классов |
Направление работы: Химия
Авторы работы: ГБОУ Школа № 1329
Email: Написать
Предметы: Химия
Классы: 10 класс
Мероприятия: Открытая городская научно-практическая конференция «Инженеры будущего» 2020 года
|
Актуальность
По данным Всемирной организации здравоохранения, в настоящее время в России увеличилась смертность от новообразований (чаще всего злокачественных), инфекционных или паразитических заболеваний. Не всегда стандартные методы лечения эффективны, поэтому одним из решений этой проблемы могут стать пептидно-нуклеиновые кислоты (ПНК), которые способны на любой стадии биосинтеза белка присоединиться к ДНК или РНК, тем самым нарушив функцию готового белка, либо сам синтез.
Цель
Синтез аденинового мономера отрицательно-заряженной ПНК на основе L-глутаминовой кислоты с циклогексильной защитой и определение эффективности данного синтеза.
Задачи
- Синтез скелета мономера ПНК.
- Конденсация защищённого аденинового производного с остовом ПНК.
- Удаление C-концевой защитной группы и оценка выхода аденинового мономера.
- Проведение 1Н-ЯМР-спектрометрии.
Оснащение и оборудование, использованное при создании работы
- Реактивы: циклогексиловый спирт, N-метилморфолин (99 %), изобутилхлорформиат (99 %), трифенилфосфин (99 %), тетрагидрофуран, изопропиловый спирт, L-глутаминовая кислота, аллиловый эфир глицина, диизопропил азодикарбоксилат, тиофенол, ацетонитрил, каталитический палладиевый комплекс, диметилформамид, морфолин, аденин-уксусная кислота, карбонат калия.
- Вещества на пластинках определяли в УФ-свете (254 нм), опрыскивая 0.5 %-м раствором нингидрина в этаноле с последующим нагреванием и раствором фосфомолибденовой кислоты с сульфатом церия (IV) (25 г фосфомолибденовой кислоты * H2O, 10 г сульфата церия (IV) * 4 H2O, 940 мл воды дистиллированной, 60 мл кислоты серной концентрированной) с последующим нагреванием.
- Колоночную хроматографию при атмосферном давлении проводили на сорбенте Silica gel 60 (0,040–0,063 мм).
- Растворители удаляли на ротационном вакуумном испарителе Heidolph WB eco при 20 мм рт. ст. (вакуум водоструйного насоса).
- Вещества сушили в высоком вакууме масляного насоса (0,5 мм рт. ст.) до постоянного веса.
- Холодильник Либиха, хроматографические колонки, круглодонные колбы (на 100 и 250 мл), трёхгорлые колбы (на 100 и 250 мл), плоскодонные колбы (на 100 и 250 мл), делительные воронки (на 100 и 250 мл), камеры для ТСХ, мерные цилиндры, роторный испаритель, вакуумный насос, УФ-лампа, штативы, лапки, магнитные мешалки, фильтры, насадки на фильтры.
Описание
а) Синтез мономера ПНК.
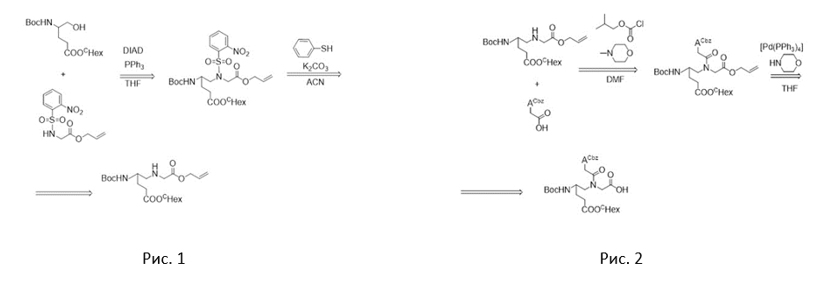
1. Синтез скелета мономера ПНК. Для синтеза скелета были проведены 2 реакции: реакция Мицунобу и тиолиз. В реакции Мицунобу между собой реагировали основание мономера и аллиловый эфир глицина, но т. к. реакция не проходит без катализаторов, то по методике взяты DIAD и PPh3, при этом THF (тетрагидрофуран) выступал в роли нейтральной среды. Далее следовал тиолиз, где происходило замещение Ns-защитной группы на водород. Катализаторами данной реакции являлись тиофенол (C6H6S) и карбонат калия (K2CO3), а ACN (ацетонитрил) – растворитель соответственно (Рис. 1).
2. Синтез целевого мономера ПНК. Для полного синтеза мономера были нужны реакции: ацилирование, проводящееся по методу смешанных ангидридов, и удаление C-концевой защитной группы. Первой была реакция ацилирования, в ней реагировали между собой синтезированный скелет мономера и клатридин А, катализаторы изобутилхлорформиат (C5H9ClO2) и N-метилморфолин (C5H11NO), DMF (диметилформамид) – среда. Далее шло удаление C-концевой защитной группы, где происходила замена защитной группы на гидроксильную. Палладиевый комплекс ([Pd(PPh3)4]) и морфолин (C4H5NO) были катализаторами реакции, а тетрагидрофуран (THF) – средой (Рис. 2). 
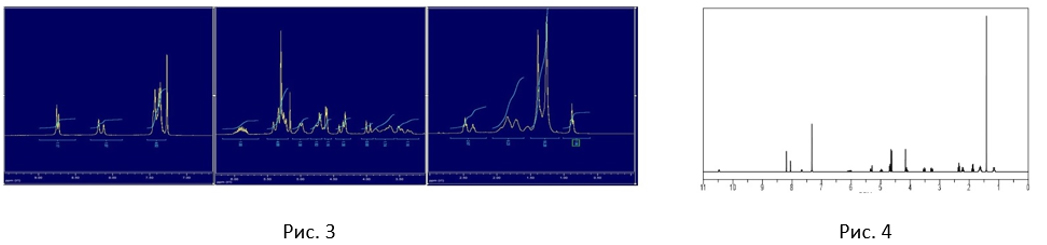
б) Проведение 1Н-ЯМР-спектрометрии.
Автор использовал метод 1Н-ЯМР-спектрометрии для подтверждения структуры полученного вещества (Рис. 3). При сравнении полученного спектра с идеальным (Рис. 4). была подтверждена структура мономера.
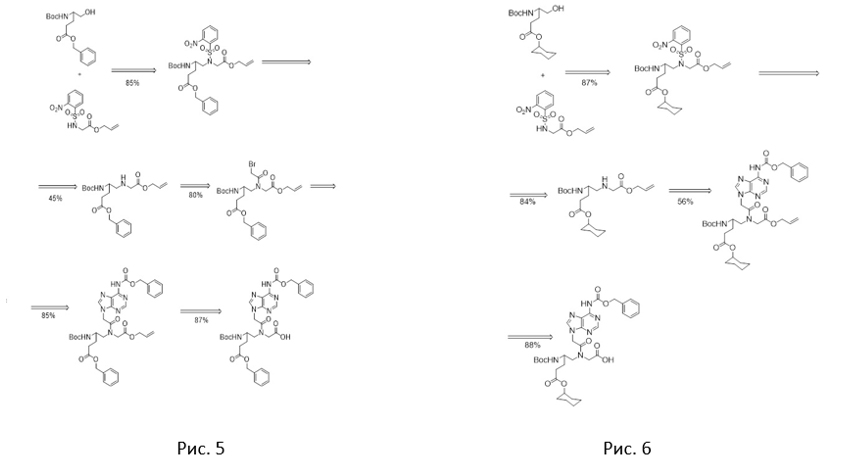
в) Сравнение общего выхода мономера с циклогексильной защитой и с бензильной защитой.
Автору была предоставлена готовая схема реакций синтеза мономера ПНК с бензильной защитой (Рис. 5), все выходы веществ (в процентах) в реакциях указаны на иллюстрациях (Рис. 5 и 6). По подсчётам общий выход мономера с бензильной защитой составил 22,6 %, а мономера с циклогексильной защитой – 36 %, что в полтора раза больше.
Результаты работы/выводы
Был синтезирован адениновый мономер с циклогексильной защитой. Его выход в полтора раза выше, чем у мономера с бензильной защитой, также этот мономер проще синтезировать.
Перспективы использования результатов работы
ПНК можно будет использовать для лечения и обнаружения генетических, вирусных, раковых или бактериальных заболеваний.
Сотрудничество с вузом/учреждением при создании работы
РТУ МИРЭА
Мнение автора
«Это был поистине тяжёлый и кропотливый труд, но проект получился очень интересным. Я рада, что смогла доделать всю работу до конца. Ты не просто делаешь всем известные опыты, а проводишь своё научное исследование наравне с настоящими учёными. Подобный опыт работы для школьника может помочь при выборе профессии. Также это позволяет понять, что наука – очень интересная сфера деятельности»
- Сборник проектных и исследовательских работ победителей и призёров открытой городской научно-практической конференции «Инженеры будущего» 2024 года
- Сборник проектных и исследовательских работ победителей и призёров открытой городской научно-практической конференции «Инженеры будущего» 2023 года
- Сборник проектных и исследовательских работ победителей и призёров открытой городской научно-практической конференции «Инженеры будущего» 2021 года
- Каталог проектных и исследовательских работ участников, победителей и призеров открытых городских научно-практических конференций 2019 года
- Энергия моря: «Морской змей»
- Анализ влияния покрытия на эффективность солнечных элементов
- Сайт мониторинга энергобаланса энергоактивного здания (GREEN SITE)
- Электролиз. Генератор водорода
- Модификация ветрогенератора
- Исследование возможности использования ветрогенераторов в мегаполисе
- Эпоксидная смола и её взаимодействие с разными факторами
- Зелёный водород – основа энергетики будущего
- Приливная электростанция (ПЭС)
- Получение «зелёного» водорода на ГЭС с использованием новых наноматериалов
- «Зелёный» бойлер – нагреватель на основе возобновляемых источников энергии (GREEN BOILER)
- Создание водородного реактора своими руками
- Умная подсветка лестничных пролётов
- Оценка механических свойств перспективного паяного соединения вольфрам/сталь применительно к термоядерному реактору DEMO
- Применение электронного прогибомера для фиксации перемещений пролётного строения при мониторинге продольной надвижки
- Система обеспечения современного дома сжатым воздухом
- «Зелёная школа» – энергоактивное здание будущего (GREEN SCHOOL)
- Создание мобильной высокомощной солнечной панели для походных условий
- Моделирование архитектурных украшений Исаакиевского собора
- Модульная муравьиная цивилизация
- Влияние сточных вод аэродрома на рост микрозелени
- Экономическая игра
- Дизайнерские часы с ночной подсветкой, будильником, возможностью выбора часового формата
- Создание дизайн-проекта «Лаунж-зона» в школе старшеклассников
- Разработка экспресс-теста на глютен методом иммунохроматографического анализа
- Исследование влияния замещения ионов Ca2+ на Sr2+ на биологическую совместимость октакальций фосфата in vitro
- Получение и изучение новых антипиренов, модифицированных нано-TiO2∙nH2O
- Новые железосодержащие наноматериалы для очистки воды
- Аптечка первой помощи, укомплектованная антисептическими полимерными материалами
- Получение изоиндолкарбоновых кислот для их тестирования на противомикробную активность
- Дезодорация и дезинфекция воздуха в школьных помещениях при помощи органических фильтров
- Синтез холестериновых производных анти-ВИЧ-нуклеозидов в качестве перспективных ингибиторов обратной транскриптазы ВИЧ
- Исследование коллоидных растворов нитрида титана и серебра, полученных методом фемтосекундной лазерной абляции в жидкости, как наносенсибилизаторов для борьбы с онкологическими заболеваниями
- Метатезисный селенсодержащий рутениевый катализатор полимеризации
- Разработка альтернативных методик удаления пятен с поверхности ткани и анализ их эффективности
- Оценка микропластика как угрозы планетарного масштаба на примере исследований бутилированной воды
- Выделение лишайниковых кислот и создание косметического средства на их основе
- Использование в арт-индустрии метода гальванопластики органических тканей на примере омеднения скелетированных листьев растений
- Восстановленный оксид графена как анодный материал для металл-ионных аккумуляторов
- Синтез гидрофобного вектора на основе дипальмитоил-амино-пропан-2-ола для создания пролекарственных производных нуклеозидных препаратов с выраженной анти-ВИЧ-активностью
- Эффективность применения полимерной биоразлагаемой подложки для увеличения скорости прорастания сельскохозяйственных культур
- Определение растворённого кислорода в суккулентах различных видов методом Винклера
- Влияние концентрации источников углерода и азота в среде на рост бактерии Methylorubrum extorquens
- Получение защитных покрытий на низкоуглеродистой стали в нейтральном нитратном оксидирующем растворе с добавками мочевины
- Баллистическая оболочка туловища из углеарамида
- Термоиндуцированное сжатие полиэлектролитных капсул с магнитными наночастицами в оболочке
- Поиск возможности биоразложения композитов на основе полиэтилена и крахмала
- Свободные радикалы в волосах человека и их изменение при химической и термической обработке
- Предложения по принципиальной конструкции универсальной энергонезависимой установки для очистки воды из родников
- Выделение и исследование наночастиц городской пыли Москвы
- Регенеративный патрон на основе пероксо-модифицированного нано-TiO2
- Экоскейт. Использование вторсырья в изготовлении скейт-досок в домашних условиях
- Разработка интерактивной зоны на территории школы с элементами ландшафтного дизайна
- Звуковая волна
- Усовершенствованный вариант тисков Моксона
- Модернизация системы вентиляции и кондиционирования воздуха здания школы
- Утилизация и вторичное использование отходов резинотехнических изделий (на примере стирательных резинок)
- Обустройство воинского мемориала в деревне Веригино
- Использование витражной росписи как одного из элементов декорирования интерьера (на примере столовой ГБОУ Школа № 2005)
- Экокрыша школы будущего
- Создание лекарственного средства, не проявляющего гепатотоксичность, на основе парацетамола и глутатиона
- Разработка плёночных съедобных биоразлагаемых покрытий на основе хитозана
- Улучшение качеств хитозана посредством модификации
- Разработка термостабильного состава для ПЦР-наборов
- Система управления водоснабжением дачного участка
- Ветроархитектура
- Скейт-парк
- Разработка и создание дизайна IT-полигона школы № 1573
- Школьная среда как элемент социального конструктора
- Синтез и свойства 1,5-диметил-3,7-дизабицикло[3.3.1] нонан-9-она
- Сравнение методов пробоподготовки при определении подвижных форм металлов в почвах
- Создание школьного спектрофотометра на основе Arduino
- Роторная парковка карусельного типа
- Возможности химиотерапии: синтез цитоксических соединений платины
- Методика нанесения защитной маркировки документов с помощью флуоресцентных красителей
- Место ли пластику в косметике?
- Создание фильтрационных половолоконных мембран для фракционирования плазмозаменителей крови
- Радиационная безопасность в школе: измерение ионизирующих излучений и комплексный анализ
- Разработка брендбука ГБОУ Школа № 64
- Влияние электромагнитного излучения мобильных телефонов на людей
- Разработка автономной системы охлаждения лабораторного холодильника
- Ультразвук служит человеку
- И светит, и греет, или Как определить удельную теплоту сгорания топлива
- Изучение состояния воды в сухих ингредиентах спортивного питания методом ЯРМ
- Устройство оповещения о звуковых сигналах с помощью вибраций для неслышащих людей
- Анализ статистики потребления вредных продуктов, влияющих на возникновение рисков сахарного диабета среди подростков и начало прогнозирования на основании использования больших данных
- Рефлексометр. Измерение простой и дифференцировочной сенсомоторной реакции человека
- Изучение явления биений и его применение
- Дистанционное зондирование Земли
- Хранение мяса в условиях акустической заморозки и оценка его биотоксичности
- Макет футбольного поля с системой освещения на основе пьезоэлементов
- Разработка действующей модели автоматической поворотной двери с кинематикой Клеменса Торглера для IT-полигона
- Беседка для внутреннего дворика школы № 1195
- Игра «ANIMAL KEEPERS»
- Проект зонирования музейно-выставочного пространства «Корабль сказок»
- Модель дома из акрила с использованием 3D-печати
- Сегментация повреждений лёгких на КТ-снимках
- Протезирование кистей рук
- Автоматизированное взятие биоматериала с использованием системы технического зрения
- Навигационный прибор для слабовидящих и незрячих людей
- Разработка тренажёра для подготовки мышц к использованию бионического протеза
- Фотолитографический синтезатор олигонуклеотидов
- Медицинская маска и ген ACE2 – внешняя и внутренняя защита от COVID19
- Накладка на клавиатуру для людей с ограниченными зрительными возможностями
- Создание 3D-модели сцены по фотографии
- Клавиатура истинного разработчика
- Изменение магнитных свойств нанопроводов в зависимости от условий их получения
- Определение коэффициента трения качения методом наклонного маятника
- Пьезоэлектрическое напольное покрытие
- Маятники в искусстве
- Разработка технологического процесса изготовления камер сгорания для ЖРД малой тяги (14 кгс) с применением композиционных материалов
- Компьютерная лабораторная работа по изучению климата Земли на примере зонального распределения температуры
- Действующий макет гидравлического манипулятора
- Изучение теплопроводности различных материалов
- Формирование отчёта по лабораторным работам
- Осциллоскоп
- Изучение информации о ГЭС. Создание макета ГЭС
- Визуализация баллистического движения в Excel
- Технология сохранения свойств и особенностей белого камня (известняка) при реставрации и консервации памятников архитектуры
- Кинетическая обучающая проун-модель «Физика»
- Инновационный метод борьбы с синантропной флорой транспортных путей на примере борщевика Сосновского с помощью растений-ремедиаторов
- Двухэтапный метод измерения, визуализации и идентификации источников переменных электромагнитных полей путём картирования и спектрального анализа
- Создание устройства для наблюдения «живой» доменной структуры в ферромагнитных плёнках
- Приобретение навыков получения высокого переменного напряжения. Передача энергии без проводников
- Синтез и исследование коллоидных наночастиц нитрида титана для применения в биомедицине
- Система управления антенной при измерении параметров электромагнитных полей в целях технической защиты телекоммуникационной информации
- Перестраиваемый экран по принципу Бабине на основе метаматериалов
- Изучение газодинамической неустойчивости Кельвина – Гельмгольца с помощью гофрированной трубы
- Система автоматической газовой сигнализации
- Импульсный ускоритель масс и его применение для устранения космического мусора
- Автополив «AgroID»
- Разработка гидроакустической навигационной системы как способа беспроводной подводной связи
- Создание твитеров для воспроизведения высокочастотных звуков в составе домашней акустической системы
- Куртка с указателями направления движения
- Энергосбережение при освещении теплиц
- Пускозарядное устройство с расширенным функционалом
- Умная ваза
- Перспективная микропроцессорная модель управления СЦБ на железной дороге
- Проект настольного акрилового светильника с функцией подставки под мобильные устройства
- Создание полупроводниковой электроники плазменными методами
- Плата для источников бесперебойного питания
- Автоматизированная система контроля и поддержания нормы температуры и влажности в кабинетах школ
- Рабочая модель катушки Теслы
- Создание пожарного робота для работ в трудных условиях
- Отвод конденсата от кондиционера с помощью технологии ультразвукового испарения
- Программируемая RGB-кольцевая лампа на основе адресной светодиодной ленты
- Разработка стенда для тестирования ВМГ
- Применение комбинированного соединения обмоток в асинхронном электродвигателе
- Крепкая бумага
- Исследование наночастиц серебра и их применение в медицинских имплантах
- Исследование эффективности автономного хладогенератора для жидкостей
- Определение наиболее выгодного метода отопления жилого дома
- Увеличение мобильности инвалидов в городской местности
- Протез ноги из углепластика
- Проектирование устройства для криоконсервации крови на основе элемента Пельтье
- Создание модели БПЛА для обучения детей младшего школьного возраста основам пилотирования и развития у них интереса к авиации
- Создание установки для исследования теплопотерь различных материалов
- Технология создания макета «Дорога жизни»
- Создание модели школы и пришкольной территории в 3D-формате
- Умная зимняя теплица
- Создание практикума по теме «Постоянный электрический ток» с использованием модернизированных реохордов
- Исследовательская работа «Принцип композитности»
- Сравнительный анализ методов радиоволнового лифтинга, применяемого в современной косметологии
- Модернизация автоматического освежителя воздуха
- Сборка лампового гитарного усилителя и исследование принципа работы лампового усилителя звука
- Разработка и создание лампово-полупроводниковой радиолы
- Подводный робот для забора проб воды и грунта
- Разработка миниатюрного ультразвукового дальномера с цифровым дисплеем на базе Arduino для проведения измерений расстояний от точки до точки
- Умная теплица
- Создание автоматизированной системы полива комнатных растений
- Автоматизированная система для теплицы
- Создание системы для автоматической подачи корма и воды домашним декоративным птицам
- Водородный электролизёр с повышенным КПД
- Интерактивная таблетница на базе Arduino
- Интерактивный макет умного дома с реализацией управления через веб-интерфейс
- Браслет-поводырь
- Разработка модели бытовой сигнализации
- Создание аппаратной платформы для развивающих игр с RFID-полем
- Умный смеситель
- Изготовление форм методом вакуумного формования
- Разработка стабилизатора напряжения для питания полезной нагрузки малого космического аппарата
- Разработка системы управления гидропонной установкой
- Указатель курса ветра для обучения управления парусными судами
- Автоматическая система учёта времени на научных судах
- Система повышения безопасности велосипедиста на дороге
- Пляжный радар
- Домашний прибор для измерения давления, температуры и влажности
- Создание прибора для автополива растений на основе Arduino с управлением через приложение
- Терменвокс с использованием лазерных дальномеров
- Умный светильник
- Лазерная арфа
- Создание образовательного набора-конструктора для изучения темы «Алгебра логики»
- Аналитические весы для работы на научно-исследовательских судах
- Автоматическая штора с функцией накопления энергии
- Дозиметр и его принцип работы
- Система умного автополива комнатных растений
- Переносное зарядное устройство с возможностью подзарядки от солнца
- Образовательный конструктор Z80
- Создание усилителя звука для бюджетной системы звукового оповещения на небольших территориях
- Создание дешёвого и мощного регулируемого источника постоянного тока для инженеров и радиолюбителей
- Устройство измерения наполняемости мусорного контейнера
- Автоматический дозатор воды
- Система поддержания микроклимата в садовой теплице
- Устройство для помощи детям с плохо развитой моторикой и ухудшенной координацией
- Система контроля уровня воды в кулере
- Автономная система по уходу за растениями
- Гардеробот: Telegram-бот для выбора одежды по погоде
- ИнфоПост
- Конструктор диагностических систем
- Оценка потенциала территории европейской части РФ для использования солнечных батарей с помощью геоинформационных технологий
- Moscow metro as an alternative energy source / Внедрение альтернативных источников энергии на примере Московского метрополитена
- Разработка приложения для учёбы в виде визуальной новеллы
- Создание интерактивного приложения для подготовки к устному экзамену по китайскому языку (HSKK)
- Интерактивная карта народного искусства России
- Решение задачи коммивояжёра в трёхмерном пространстве
- Расшифровка языка жестов
- Использование распределённой сети при решении задач оптимизации с помощью эволюционных алгоритмов
- Приложение для учеников
- Конструкция вертикального озеленения рекреационных и учебных помещений ГБОУ Школа № 1564 «Вертикальный сад» с автоматизированным поливом для поддержания экологии школьной среды
- Автоматическая таблетница
- Контроль фильтров очистки воды
- Мобильное приложение Palladium (Цифровой завхоз)
- Создание мобильного приложения для изучения алгебры
- Mit App Inventor
- Система сигнализации на базе технологий умного дома
- Система контроля 3D-принтера посредством Телеграм-бота
- Программа «Антиплагиат» с графическим интерфейсом для файлов .txt и текстов
- Спектральный звуковой анализ в целях идентификации и классификации людей по голосу
- Генератор коллажа финишных материалов
- Автоматический распознаватель аккордов для гитары
- Навык Яндекс.Алиса Гардероб
- Безопасность цифровых активов
- Модуль анализа состояния посевов с помощью NDVI
- Кибербезопасность. Сетевые атаки
- Приложение для обработки фотографий, реализованное на языке программирования Python
- Анализ отзывов клиентов на банковские каналы обслуживания и продукты/услуги
- Искусственный интеллект для нашей теплицы
- Создание универсального интерфейса для работы с базами данных
- Чат-бот «Notify.Manga»
- LaTeX-редактор
- Голосовое управление для электронных шахмат
- Туристическое iOS-приложение с дополненной реальностью
- Нейронная сеть по распознаванию животных
- Интернет-ресурс «We-ask» – форум начинающих программистов
- Счёт на пальцах
- Умный дом. Умный свет
- Мобильное приложение для удалённого управления компьютером
- Разработка алгоритма распознавания жестов, применимого для систем компьютерного зрения и smart-перчатки
- Умное зеркало – будущее вашего дома
- Web-приложение для создания и обмена визитками
- Моделирование полёта космического аппарата
- Web-страница с информацией о потребительских качествах и физических свойствах компьютерных комплектующих
- Умный дом. Электросети загородного дома
- «Robot store»
- Анимация как инструмент восприятия информации подростками
- Приложение для расширения словарного запаса
- Рабочая тетрадь для виртуальных лабораторных работ
- Прибор для измерения скорости ветра (Анемометр)
- Создание прототипа интуитивной системы контроля над распространением коронавирусной инфекции в школьной среде
- Сервис для обучения основам алгоритмики. Машина Тьюринга
- Чат-бот для помощи в подготовке к итоговому сочинению
- Приложение для быстрой оплаты через «Систему быстрых платежей»
- АСВК-олимпиада (автоматизированная система выдачи ключей Всероссийской олимпиады школьников)
- Создание универсального приложения для записей, заметок и конспектов
- Автоматизация создания школьного расписания
- Разработка многофакторной аутентификации с применением электромеханического замка на основе GSM-модуля
- Приложение для отдыха и психологической поддержки
- Мобильное приложение для изучения китайских слов
- Telegram-бот для выявления дизорфографии
- Сервис для интеллектуального аннотирования (суммаризации) текста
- Создание нейронной сети для реставрации древнерусской иконописи
- Бот «Электрон»
- Web-приложение для заказа пропусков на территорию охраняемых объектов
- Искусственный интеллект для прогноза результатов спортивных матчей
- Разработка сайта для дизайнера
- Чат-бот «Школьник»: расписание класса, научные факты, теория по ключевым предметам – в твоём кармане!
- Разработка Telegram-бота для администрирования теннисной школы
- Реализация чат-бота в Telegram для решения задач по системам счисления: от простых до олимпиадных
- Устройство для распознавания лиц на энергоэффективных ядрах
- Создание информационного ресурса для обучения игры в баскетбол
- Webudget. Приложение для контроля повседневных расходов
- Распознавание автомобильных номеров
- Система помощи по соблюдению масочного режима на основе анализа видеопотока
- Компьютерное моделирование долгих прогулок с домашними животными: автоматический расчёт времени и пройденного пути, определение усталости в конце прогулки
- Дискорд-бот для обучения
- Simple Messenger
- Программа-ассистент для организации проектной деятельности
- Система мониторинга газоводоснабжения в помещении
- Разработка менеджера паролей «Tessera»
- Создание альтернативного метода шифрования
- Образовательный чат-бот по решению задач на круги Эйлера, реализованный на языке программирования Python
- Мобильное приложение «Пожарка»
- Интеллектуальная система распознавания лиц
- Разработка Телеграм-бота по профессиональной ориентации детей в сфере космонавтики на основе метода Дж. Голланда
- Система умных парт «SmartTab»
- Система аутентификации в образовательных учреждениях
- Разработка Web-приложения для изучения корейского языка в интерактивной форме
- Приложение для отслеживания присутствия на дистанционном уроке
- Пособие «Круговорот воды в природе» для слабовидящих детей
- Создание учебного пособия «Интерактивный музей следов зверей и птиц»
- Автоматизированный комплекс для химического анализа донных осадков
- Управление микроконтроллером ESP 32 CAM дистанционно с помощью интернет-ресурсов
- Разработка телеуправляемого необитаемого подводного аппарата как средства мониторинга состояния водных ресурсов
- Разработка автоматической линии по производству кондитерских изделий
- 3D-модель ДВС
- Разработка наглядного пособия по физике на основе конструкции Тенсегрити
- Миниатюрный станок с ЧПУ для фрезеровки печатных плат
- Создание инженерных лабораторий для поддержания работоспособности школьного оборудования
- Робот-кондиционер
- Модель плёночного фотоаппарата
- Мой манипулятор
- Управляемый штатив для съёмки фото и видео на телефон
- Настольная игра, адаптированная для незрячих и слабовидящих детей
- Модели двигателя внутреннего сгорания
- Штанга, выполненная из сверхпрочного композиционного материала, для крепления гибкой солнечной батареи космического спутника
- Автоматизация процесса диорамной съёмки в покадровой анимации
- Панобот
- 3D-сканер с использованием микроконтроллера Arduino
- WebLabory
- Создание 3D-пособий для слабовидящих детей
- Современный да Винчи
- Робот – уборщик игрушек
- Сервис для моделирования поведения и программирования квадрокоптеров в облачной среде «COEX-Cloud»
- Создание системы для улучшения досуга людей с ограниченными возможностями
- RoboAnt – многоцелевые роботы на базе универсальной шагающей платформы
- Универсальная платформа шагающего робота «КОТ»
- Создание головоломок в Autodesk Inventor Pro 2021
- Настольная игра «Пожелание»
- Шлем для альпинизма, выполненный из сверхпрочного композиционного материала
- Создание облегчённой ракетки для настольного тенниса, выполненной из сверхлёгких композиционных материалов
- Изготовление мастер-модели гребного винта
- Дорожные приключения
- Приложение для обмена опытом по профессиям
- Создание бота-консультанта в Telegram
- Информационное агрегирование волонтёрской деятельности по жизнеобеспечению бездомных животных
- Мобильное приложение – помощник в утилизации мусора
- Синхронизация полёта группы БПЛА
- Сопоставление эффективности методов оптимизации и уравнений при описании зависимостей избыточной мольной энергии Гиббса в бинарном растворе
- System of periodic body temperature monitoring under pandemic conditions based on a medical mask holder for educational organization employees/Система периодического мониторинга температуры тела сотрудников образовательной организации на основе держателя
- Creation of the interactive models for Moscow Electronic School with «1C: Mathematical Constructor» / Создание интерактивных моделей для московской электронной школы в программе «1С: Математический конструктор»
- Система ограничения скорости самоката
- Умная ёмкость
- Автоматизация гардероба
- Сайт с интерактивной таблицей Менделеева
- Генератор вариантов задач по алгебре для 8 класса с пятью уровнями сложности
- Создание учебно-методического модуля в предметной области химии
- Разработка и изготовление методом FDM-печати модели прототипа «Ополаскиватель для химической посуды» при помощи систем быстрого прототипирования
- Косметическая накладка анатомической формы для механизированного протеза ноги, выполненная с применением аддитивных технологий и реверс-инжиниринга
- Создание 3D-модели стартового пистолета с рабочим ударно-спусковым механизмом
- Сборно-разборная модель тазовой кости человека
- Использование аддитивных технологий при создании СВЧ-устройств
- Sкедуль
- Макет мобильного приложения «Моя культура»
- Hobynizer – удобный органайзер для вашего хобби
- Проектирование и изготовление композитного рюкзака
- Бионический протез человеческой руки на 3D-принтере
- На уроке физики был взрыв
- Речевое оповещение о приезде общественного транспорта
- Автоматизированная система мониторинга осанки человека
- Remember Bot – чат-бот школьного дневника
- Система обеспечения безопасности людей и транспорта на парковках в холодное время года
- Умное зеркало для отслеживания расписания
- «Смомби»: проблемы и решения
- Автоматический бесконтактный термометр АБТ-2100
- Создание обучающих видео для курса «Космическая вёрстка»
- Разработка web-приложения для повышения успеваемости учащихся через увеличение концентрации внимания
- Умная система прохода для учебных учреждений «NFC KEY»
- Устройство для экономии/контроля воды
- Система автоматического обнаружения неисправности электроосветительных приборов и подтопления подвальных помещений
- Система предотвращения происшествий во время движения спецтранспорта на перекрёстке
- Создание учебной модели ДНК для уроков биологии профильного уровня
- Сайт для помощи выбора прически «HairBrush»
- Создание приложения для поиска рецептов и организация взаимодействия авторов рецептов
- Система автоматизированного температурно-пропускного контроля (САТПК)
- Телеграм-бот для шифрования
- Термометрическая подставка
- Мобильное приложение экстренной помощи
- Вас распознали: автозаполнение посещаемости на основе распознавания лиц людей
- Разработка исследовательского микроспутника
- Создание леденцов на основе ягод клюквы болотной («Oxycoccus palustris») как источник иода для детского организма
- Разработка школьного транспортировщика питьевой воды
- Автоматизированный комплекс по сортировке мусора
- Телеметрическая система грузового железнодорожного вагона
- Роботизированный краулер
- Разработка контрольно-сортировочного автомата
- О возможностях и преимуществах применения компьютерного моделирования при испытаниях грузового подвижного состава
- Багги-карт
- Руль болида из композиционных материалов
- Создание электромагнитной установки для очистки околоземной орбиты от космического мусора
- Умный дом
- Исследование способов уменьшения сопротивления воздуха в закрытых пространствах за счёт вращательного движения
- Проект крепления противоугонного устройства велосипеда
- Разработка и создание полноприводного шасси радиоуправляемой модели автомобиля
- Ленточный станок гриндер
- Повышение городской и межгородской мобильности при помощи гравитационного транспорта
- Создание автономного необитаемого аппарата для подводной диагностики
- Проектирование радиационной защиты для головного обтекателя космического корабля
- Держатель коляски в общественном месте
- Оптимизация левого поворота у беспилотных автомобилей
- Создание действующей модели автомата перекоса тарельчатого типа для изучения процесса управления вертолётом
- Изготовление изделия из композитных материалов методом вакуумной инфузии. Открытие промышленного цеха
- Разработка универсальной манёвренной платформы
- Применение действующего кинетического стола и кинетической ленты как транспортной системы
- Влияние авиационного топлива на искусственное покрытие аэродрома
- Программа сравнительной оценки методов очистки светлых нефтепродуктов от примесей серы и сероводорода
- Живое яблоко
- Снегоболотоход. Разработка вездехода с эффективными и устойчивыми к низким
- Макет ж/д-переезда
- Цифровая тяговая подстанция
- Wise-soft – подвеска настоящего будущего инженера
- Чат-бот в Telegram для решения задач на графы
- Программа для подготовки к ОГЭ по математике «Остров Математики»
- Создание мобильного приложения «Музыкальный диктант»
- Школьная система хранения гаджетов
- Моделирование историко-архитектурной среды города с использованием геоинформационных систем и пакетов трёхмерной графики
- 3D-модель «Музыкальная шкатулка-рояль»
- Автоматическая межпланетная станция
- Создание прототипа бронежилета
- Создание модели кривошипно-шатунного механизма
- Проектирование мультимедийного приложения «Evology» с элементами дополненной реальности
- Прототип робота-снегоуборщика
- Разработка специальной одежды для людей с ОВЗ
- Мобильный медицинский робот для красных зон
- Система контроля школьников на выездных мероприятиях
- Интерактивная 3D-модель школы
- Концепт автобусной остановки «Аура»
- Интерактивный макет вагона метро
- Противоударная хоккейная маска
- 3D-модель роторного двигателя
- Создание прототипа домашнего ирригатора
- Создание набора улучшений к лазерным станкам с ЧПУ
- Разработка и визуализация оригинального дизайна рабочего места
- Модель турбореактивного двигателя
- Изготовление индивидуальных деталей для автомобиля
- Пособие-игра «3D-REBUS» с использованием AR-технологий
- Унификация игры «Зельеварение» с помощью 3D-моделирования
- Модель устройства для переплавки пластиковых отходов в нить для 3D-печати
- Фотопанорамные 3D-VR туры на примере проектов «Виртуальный музей Московского метрополитена», «Вечерняя Москва», «Павильон авиации и космонавтики № 34, ВДНХ»
- Использование аддитивных технологий в преподавании черчения
- Солнечная система в дополненной реальности
- Создание симулятора выживания в виртуальной реальности
- Изготовление модели ордена Святой Великомученицы Екатерины на 3D-принтере
- Доступная модель протеза ноги на 3D-принтере
- Создание экспоната для школьного музея «Мастер танковых ударов» пулемёт ДТ-29
- Запорно-регулирующая арматура
- Автономная уличная система кормления для животных
- Устройство для контроля осанки
- Создание экспериментальной модели робота-эколога для мониторинга лесов
- Опорно-поворотная платформа с модулем наведения антенны
- Робот, объезжающий препятствия с помощью ультразвукового датчика расстояния
- Беспилотный летательный аппарат и система управления им, основанная на Arduino
- Искусственный интеллект своими руками
- Использование современных материалов и технологий при конструировании спортивной авиамодели
- HelpUnicorn: платформа для IT-помощи благотворительным организациям
- Применение обратной теоремы Пифагора для определения вида треугольника
- Робот-Колобок
- Устройство контроля и поддержания оптимального микроклимата в учебном заведении
- Ракета
- Дрон-поисковик из сверхлёгких композиционных материалов с использованием углепластикового каркаса, бесколлекторных моторов и солнечной батареи
- Разработка робота-манипулятора с использованием омни-платформы и цепного подъёмника
- Умный медицинский робот-ассистент «ADI»
- Food Factory
- Разработка системы автоматизации внутрискладской логистики грузов
- Создание автоматической системы полива растений на загородном участке
- The backpack «Cyberbag» made of ultralight composite materials with an alarm lighting system / Рюкзак «Cyberbag», выполненный из сверхлёгких композиционных материалов, со светодиодной системой оповещения
- Система экстренного отключения подачи газа и воды
- Умный фонтан «Обитатели морских глубин»
- Умный термометр
- Визуальная новелла как подход к вовлечению изучения русской литературы, способствующий проявлять инициативность в осуществлении действий
- Устройство «Помощник для сбора рюкзака»
- Интерактивный макет умного дома с реализацией управления через веб-интерфейс
- Умная урна «UKU»
- Учебно-методический набор для изучения работы логических элементов и схем
- AR-приложение для школьных библиотек, демонстрирующее атмосферу книги – «Illustart»
- Artificial intelligence as an effective classroom assistant / Искусственный интеллект – эффективный помощник учителя
- Инновационные решения умного города
- Создание устройства для контроля состояния дорожного полотна
- Автоматизация распознавания занятости парковочных мест, отмеченных знаком 8.17
- Разработка электронных программируемых конструкторов POV-дисплея для образования и развлечения
- Модифицированный модуль для предоставления доступа к местам маломобильных и пожилых пассажиров в автобусе
- Поисковое устройство «Эврика»
- Инновационные способы изучения литературных произведений с использованием платформы izi.travel и Emaze Creative Editor, видеоредактора Movavi
- Ультразвуковой дальномер
- Организатор рабочего места
- Умный дом на Arduino (Smart House)
- «Нейродиагност» – приложение для помощи в определении диагноза (NEIRODIAGNOST)
- Прибор для контроля дыхания в домашних условиях
- Микробиологический анализ воды реки Клязьма
- Программное обеспечение для изучения работоспособности мозга
- Протез с силомоментным очувствлением
- Создание умной таблетницы «Smart Pill Box»
- Программная реализация модели сборки генома
- Изучение видового полиморфизма ДНК мяты перечной
- Идентификация хвоща полевого в сухом чайном напитке с помощью ДНК-маркёра
- Система безопасности Student Lock
- Звуки флейты сякухати донеслись из принтера
- Создание компоновочной схемы фандомата для утилизации алюминиевых банок
- Зонт «free hands»
- Анимированная 3D-модель советско-российской гусеничной десантной машины БМП-2
- Использование VR- и AR-оборудования для проведения экспериментов по физике в школах
- Устройство контроля по уходу за комнатными растениями
- Изготовление лангета для животных с использованием аддитивных технологий
- Создание 3D-моделей архитектурных элементов
- «Гибрид-1». Создание 3D-модели гибридного беспилотного летательного аппарата для многофункционального использования
- Устройство для съёмки 3D-панорамы
- Разработка школьной айдентики (Разработка фирменного логотипа. Графический дизайн)
- Приложение виртуальной реальности для релаксации и отдыха – «DistantRest»
- Применение радиоактивных отходов природного и техногенного происхождения в качестве альтернативных источников энергии
- Система адаптивного освещения
- Конструирование лодки на солнечных батареях
- Использование энергии солнца и дождевых капель в качестве альтернативного источника электроэнергии
- Приложение под виртуальную реальность для создания дизайна квартир
- «Умный» светильник
- Купол церкви из композитных материалов
- Проектирование сельских зданий и сооружений для территорий, подверженных наводнению
- Детская развивающая мебель
- Разработка дизайна подъезда многоквартирного дома
- Проектирование и разработка программного обеспечения синтеза трёхмерных моделей типовых зданий
- Концепция реконструкции площади Санта Кроче
- Микробиологическая оценка метрополитена
- Биореализуемый материал с антибактериальными свойствами для изготовления ожогового пластыря
- Качество молока
- Спектрофотометрическое исследование растворов сульфатов кобальта(II) и никеля(II)
- Разработка нанодисперсий на основе конъюгата α-липоевой кислоты и пропандиола с антиагрегационной активностью
- Влияние состава катализатора на показатели процесса дегидрирования изопропилового спирта
- Синтез производных индолил-3-масляной кислоты
- Изучение влияния условий хранения на пригодность питьевой воды
- Кто яблоко в день съедает, тот у врача не бывает
- Синтез полиглицерилфосфатов модифицированного строения как потенциальных ингибиторов адсорбции ВИЧ
- Материал и имплантат для восстановления хряща ушной раковины
- Центробежная сила. Её проявление в природе и применение в технике
- Расчётно-экспериментальное исследование баллистики страйкбольного оружия
- Заглублённые мусорные контейнеры
- Проектирование инновационной автобусной остановки для использования в городской среде
- Малые архитектурные формы – поддержка биоразнообразия на промышленных предприятиях
- Программируемая гирлянда на основе адресной светодиодной ленты
- Осуществление обучения учеников с ограниченными возможностями здоровья в общеобразовательной начальной школе
- Разработка энергоэффективной системы вентиляции и кондиционирования воздуха образовательной организации
- Проект цветника на воинском мемориале в деревне Веригино
- Опыт визуализации отдельных существующих и исчезнувших сооружений Москвы посредством программ для трёхмерного моделирования и геоинформационных систем
- Разработка настольной игры «Инженерный мир котиков»
- Практикум для решения задач ОГЭ (макет)
- Разработка новой технологии возведения сборно-разборных архитектурных сооружений
- «Умная» автобусная остановка
- Изучение процесса кавитации и возможности практического использования метода кавитации для обезвреживания и преобразования отходов заготовки и переработки древесины в полезную продукцию
- «Умная» теплица
- Автоматизация выбраковки упаковок тест-полосок для глюкометров
- «Ультралокальные» системы выращивания растений
- Автоматическая кормушка для рыб
- Разработка и создание исследовательского микроспутника
- Цветовой определитель «Color Detect»
- Изменение электрического сопротивления тензорезисторов при деформации
- Цифровой термометр
- Модифицированный датчик линии для робототехнических устройств
- Система отпугивания птиц (робот-пугало)
- Пьезоэлектрический эффект и его использование
- Многофункциональный светильник с дистанционным выбором режима работы
- Создание солнечного датчика
- Система контроля нагрузки на ось грузового автотранспорта
- Пневматическое метательное устройство для военно-тактической подготовки
- Преобразователь азбуки Морзе
- Программируемый бюджетный портативный IC-автомат для диагностики и проверки логики цифровых микросхем
- Аналитические весы для работы в условиях морской качки на научных судах
- Универсальное реле. Реле времени и термореле в одном устройстве
- Кодовый замок на релейной схеме управления и на программируемой плате Arduino
- Автоматическая система кормления для домашних животных
- Робот-рыбак
- Прототип выключателя для «умного» дома
- Разработка панели управления для комбинированного электро-твёрдотопливного котла отопления
- Кодовый замок
- Автоматизированная система выращивания растений «Smart greenhouse» с голосовым ассистентом
- Разработка кодового замка на базе микроконтроллера Arduino
- «Часы рабочего времени»
- «Умная» урна
- Создание звукового детектора электромагнитных волн
- Портативная интеллектуальная метеостанция с функцией управления «умным» домом
- Куб-компаньон для управления IoT-устройствами
- Переноска с электрообогревом
- Гитарный эффект
- Голографическая призма
- Гравитационный транспорт как новый вид городской и межгородской мобильности
- Устройство для автоматической сортировки мусора
- Роботизированный комплекс прокладки городских коммуникаций
- Проблема строительства и эксплуатации Северного широтного хода
- Аэросани
- Использование ракетоплана для формирования погодных условий
- Моделирование и прототипирование модели электромобиля «RE ROSSO E20»
- Система блокировки зажигания
- Интеллектуальная система навигации для «умного» города
- Модель гражданского самолета «ОГЛ-1»
- «Лежачий полицейский» на основе неньютоновской жидкости
- Создание прототипа универсального вездехода «ALLTER»
- Самолёт-квадрокоптер
- «Антисон 2» – устройство безопасности водителя автомобиля
- Использование дирижаблей для выполнения авиационных работ
- Генерация энергии
- Модифицированная доска для сёрфинга с подводным крылом на электрической тяге
- Мобильная буровая установка
- Создание спортивного трицикла
- «Умный» транспорт современного мегаполиса
- Двигатель Стирлинга
- Чат-бот «BotMusician»
- Автоматизированная система оповещения водителя о въезде в жилую зону
- Научная симфония: связь музыки и науки
- Модель скейтборда «эскимо» с электронным набором, выполненная из сверхлëгких композиционных материалов
- Модель первой русской подводной лодки
- Создание управляемого карт-тягача минимальной себестоимости из подручных материалов
- Внедрение холодного газодинамического напыления высокого давления в процесс ремонта турбореактивного двигателя
- Радиационная защита для космических кораблей
- Тренажёр для трейдинга
- Создание тестов для самостоятельного изучения и самоконтроля изучаемого материала
- Создание приложения-переводчика с языка программирования Pascal на язык программирования Python
- CLASSTEST – онлайн-платформа для тестирования знаний школьников
- Электронный каталог школьного музея «Добровольцы»
- Сайт зоомагазина
- Определение места жительства по социальным сетям
- «Бабушкина пряжа»
- Приложение Polymonial Calc
- Комплекс выявления неправомерной парковки транспортных средств
- Разработка умного справочника на базе Telegram-бота
- Разработка сайта для тестирования программ
- Дополненная реальность
- Платформа онлайн-тестирования
- Нахождение коэффициентов в химическом уравнении
- Скорочтение
- Здоровье школьника
- Интерактивная игра «Обезвреживание бомбы»
- Образовательный чат-бот на языке программирования Python «Тренажёр по решению комбинаторных задач и задач на множества»
- Создание бота в Discord для онлайн-мониторинга игрового профиля
- Web-технологии, dev-ops, организация сервисов, менеджмент трафика
- Социальная сеть Comject
- Картографирование железнодорожного транспорта в районе города Якутска
- Автоматическая система сортировки бытовых отходов для мусоропровода
- Арктика Interactive: создание интерактивной карты полезных ископаемых в Арктической зоне России
- Разработка программного обеспечения для генерации краткого содержимого выбранного текстового отрывка
- Виртуальная художественная 3D-галерея «Женщины в Великой Отечественной войне»
- Консольное приложение для изучения криптографических алгоритмов Crypto.App
- Сайт-форум с тематикой «Информационная безопасность»
- Создание программы «Тренажёр устного счёта: Умножение»
- Simply Food – это просто питаться правильно
- Математический тренажёр «Brain Storm»
- ALUB фоторедактор
- Создание интернет-ресурса SCHGK для поиска турниров по спортивному «Что? Где? Когда?» для школьников
- Исследование цифровых методов инженерного анализа на примере решения модельных задач
- Разработка онлайн-тренажёра для тренировки устного счёта
- Расчёт и визуализация траектории малого космического аппарата на высокоэллиптической орбите
- Android-приложение Student Assistant
- Создание Telegram-бота на языке Python для удалённого доступа к компьютеру
- Построение карты пространства на основе видео-стереопары
- Система интеллектуального мониторинга социального дистанцирования
- Разработка робота для игры в «Крестики-нолики»
- Автоматическая система ячеек для хранения личных вещей
- Робот-исследователь для видеоинспекции труднодоступных мест
- Постройка судна на беспилотном управлении
- Разработка системы навигации внутри роботизированной складской ячейки
- Оценка сокращения выбросов парниковых газов от реализации проекта в области концепции ответственного потребления
- Вирус-краудсорсинг
- Синхронизированный полёт группы БПЛА
- Продуктиндер
- Smart Mirror – зеркало «умного» дома
- «Умная» колонка с функцией «Озвучивание рецепта либо списка ингредиентов блюда по запросу»
- Электронный арбитр для интеллектуальных игр
- Усилитель работоспособности (Work Booster)
- Инженерное решение по повышению безопасности дорожного движения для велосипедистов
- «Умный» стилус
- Меню-конструктор «FOODIE»
- RGB-Плинтус
- Модульная программно-аппаратная платформа для освоения разработки микропроцессорных систем
- Школьный самокат
- Программно-аппаратный комплекс автоматизации открывания дверей
- Модернизация крытого спорткомплекса школ
- Макет онагра с системой управления голосовыми командами
- Создание теплицы с автоматическим поливом растений
- Динамика изменения показателей качества воды в роднике № 39 Тропарёвского лесопарка г. Москвы. Предложения по внедрению энергонезависимой системы очистки родника
- Эффект магнитной левитации на основе 3D-моделирования
- Робототехнический конструктор на базе платформы Ардуино
- Создание учебного 3D-макета человеческого зуба для уроков биологии
- Школьный музей с применением AR-технологии (Augmented Reality)
- Основные этапы проектирования, разработки и реализации шлифовального станка с использованием 3D-моделирования
- За страницами учебника геометрии: дополненная реальность
- Мобильный учебный класс для изучения астрофизики
- AR-технологии и их использование
- Интерактивная модель таблицы Д.И. Менделеева в AR
- «Умная» защита от протечек (УЗОП)
- Инвалидная коляска с функцией спуска и подъема по лестнице
- Автоматизированный помощник «ТОЧКА» для занятий рисованием
- Инновация накопителей: как сделать энергосистему более гибкой, дешёвой и экологичной?
- Контроль доступа по биометрическим параметрам
- Сравнительный анализ содержания «живых» лактобактерий в молочных продуктах на примере йогуртов различных производителей
- Исследование методов мультиклассификации клеток костного мозга
- Проектирование и изготовление композитного рюкзака
- Web-сервис для тренировки межпредметных знаний в игровой форме
- Викторина на знание среды программирования Scratch
- Разработка программы для прохождения аудита на соответствие двум стандартам информационной безопасности для российских и международных платежных систем
- Разработка распределённой системы дистанционного мониторинга уровня воды в кулерах
- Генерация отзыва о вузе при помощи Telegram-бота
- Создание квест-игры по заданиям ОГЭ по математике
- Разработка чат-бота для взаимодействия с расписанием школы
- Web-сервис для оперативного обмена исходным кодом
- Компьютерная система обработки текста, содержащего нецензурную лексику
- Сурдо-тренажёр (СТ)
- Мобильное приложение «Рецепт из подручных ингредиентов»
- Создание устройства для лиц с нарушениями зрения, помогающего ориентироваться на местности
- 3D-корсет (для травмированных конечностей)
- «Умный» город. Улучшение транспортной доступности в районе Нагатинский затон
- Дизайн-проект многофункционального школьного помещения
- Создание цифровой 3D-модели микрорайона
- Создание AR-модели «Солнечная система» с возможностью реализации приложения в МЭШ
- 3D-принтер Prusart
- Приложение виртуальной реальности для сборки электрических схем
- Информационный стенд об экологии в дополненной реальности
- 3D-модель беседки из вторсырья (поддонов, палет)
- «Умный» обогреватель
- Автоматизированный вагон метро
- Умный свет
- Создание виртуального музея физических приборов
- Интерактивный фонтан у северного выхода станции метро «ЦСКА»
- Дрон-доставщик
- Макет «вечного двигателя»
- Разработка украшения-носителя в Вlender
- Разработка интерактивных лабораторных работ
- Приложение дополненной реальности «Geometry AR»
- Создание удобного стационарного фена для людей с ограниченными возможностями
- Система поддержки передвижения маломобильных людей «Попутчик»
- Разработка модели персонажа для игры жанра rougelike
- Цифровой образовательный продукт «PAUTINA»
- Светофор с датчиком движения
- Чат-бот Telegram по подготовке к экзамену по английскому языку
- Автоматизированная система для проветривания помещений
- Роль пластика в загрязнении окружающей среды, мой вариант его вторичного использования
- Видеоэкология – наука для жизни
- Противоопухолевый комплекс олова на основе глицирризиновой кислоты
- Вода, которую мы пьём. Универсальный прибор для очистки воды
- Синтез альфа-линоленовой кислоты. Создание эмульсии на основе ненасыщенных жирных кислот
- Объединение нанотехнологий и наноматериалов с полимерами с целью получения полимеров с новыми свойствами
- Разработка методики сравнения антиоксидантной активности эфирных масел сосны и апельсина
- Химический состав бальзама для волос: влияние компонентов состава на структуру волоса
- Составление технологического справочника с целью дальнейшего использования на производстве
- Синтез и подтверждение структуры перспективного противогрибкового агента
- Компактный водородный реактор
- Подбор физико-химических условий для повышения КПД микробного топливного элемента – перспективного источника энергии на предприятиях
- Фильтрация микрочастиц
- Получение антибактериального композита на основе нанотрубок галлуазита
- Синтез 1,3-дипальмитоилглицерина и гидрофобного вектора на его основе
- Комбинирование анионных и неионогенных смачивателей для использования в лакокрасочных рецептурах
- Получение и изучение новых антипиренов, модифицированных нано-TiO2∙nH2O
- Новые железосодержащие материалы для очистки воды
- Почему возникают тайфуны, или Нагреваем воду сверху
- Учебное пособие-модель «Теллурий»
- Рефлектор зеркальных космических антенн межспутниковой связи из композиционных материалов
- Распространение лазерного излучения в оптически неоднородных жидких средах: на примере явления «ФАТА-МОРГАНА»
- Дискретный теплоаккумулятор, устройство для накопления тепла и передачи его внешнему объекту
- Исследование концентрации углекислого газа в помещениях
- Автоматизированная мобильная система кормления крупного рогатого скота
- Исследование магнитооптических свойств феррит-гранатов с различными примесями
- Определение механических характеристик разработанного многокомпонентного сплава на основе алюминия и возможности его использования в качестве материала автомобильного диска методом компьютерного моделирования
- Автоматизация предметного столика поляризационного микроскопа
- GeoGebra. Виртуальный стенд для интерактивных физических демонстраций по разделу «Геометрическая оптика»
- Ветровой генератор как альтернативный источник электроэнергии в загородном доме
- Многоканальная система автоматического полива растений
- 3D-левитрон. Установка для создания стоячих звуковых волн
- Определение нагрузочной характеристики контактного датчика силы
- Поиск оптимальных параметров выращивания скелетных кристаллов висмута
- Проект ракеты с твердотопливным двигателем
- Микрогидроэлектростанция своими руками
- Портативный прибор для измерения сердцебиения плода
- Автоматическая система управления отоплением загородного дома
- Гальванически изолированная система управления мощным источником питания
- Специальный коврик с беспроводной зарядкой
- Специальная система для считывания текста Брайля и последующего его перевода в латиницу и кириллицу
- Манипулятор в виде человеческой руки с отдачей ощущений
- Роботизированный комплекс для химического анализа донных осадков
- Устройство автоматической стабилизации и контроля беспилотного летательного аппарата SILF
- Bio-Hatchery Helper
- Роботизированный подводный аппарат
- Разработка прибора для измерения параметров воздушной среды
- 3D-анимация скелетной мускулатуры тела штангиста
- Помощник слабослышащего – электронное ухо (Electronic Ear)
- Разработка мобильного бинарного комплекса «TASF» видеофиксации состояния территориально распределенных объектов
- Разработка прототипа устройства для тестирования программ управления автономным полётом беспилотного летательного аппарата
- Автоматизированный террариум «Hometerra»
- Разработка прототипа кобуры для страйкбольного пистолета Glock
- Разработка и демонстрация функционирования системы мониторинга состояния человека в специальных стационарах
- Храм Иконы Владимирской Божией Матери
- Робот для прокладки коммуникаций «TechnoWorm D200»
- Бесконтактный санитайзер
- Создание 3D-пособий для слабовидящих детей «Alias» по-новому»
- Энергия моря: Морской змей
- Внедрение альтернативных источников энергии на примере метрополитена
- Разработка и создание управляемой модели двухосной системы ориентации солнечных панелей
- Система безопасного освещения лестничных пролётов
- Солнечный чехол для зарядки смартфона (Solar Case)
- Виртуальный мебельный магазин
- Витражная роспись как способ декорирования интерьера школьной столовой (на примере ГБОУ Школа № 2005)
- Проектирование 3D-модели современной школьной столовой
- Разработка модели мобильной осветительной системы
- Разработка школьной айдентики
- Сравнение концентрации каротиноидов в моркови и в филе рыбы семейства лососёвых
- Экспрессное профилирование жирных кислот в плазме крови человека методом масс-спектрометрии MALDI
- Создание универсального термоинтерфейса
- Получение бальзама для губ в домашних условиях
- Синтез и строение координационных полимеров переходных металлов с анионами замещённых малоновых кислот и мостиковыми N-донорными лигандами
- Изучение срока годности сока в пакете после вскрытия по микробиологическим показателям
- Новые матричные соединения для экспрессного детектирования действующих веществ в лекарственных формах методом масс-спектрометрии MALDI
- Получение экологичных строительных материалов с водоотталкивающими и противогрибковыми свойствами
- Безопасное производство с применением аммиака
- Многоразовые, высокоэффективные тест-полоски для глюкометра
- Создание противоопухолевого препарата на основе природного хлорина и соединений платины
- Синтез нано-Ag и получение на его основе полиакрилатных противоожоговых гидрогелей
- Создание одноступенчатой ракеты и исследование её аэродинамических свойств
- Способ автоматического регулирования плотности раствора и программное обеспечение автоматического управления технологическим процессом
- Физика в играх
- Исследование пределов реализации течения коанда и образования зоны турбулентности при обтекании цилиндрических тел с помощью объекта science art «незаметная бутылка»
- Лабораторная установка для измерения скорости звука
- Возможный способ реализации термодинамического эффекта извлечения влаги из воздуха методом конденсации в задаче индивидуального обеспечения водой личных подсобных хозяйств в условиях Крымского полуострова
- Разработка метода генерации электроэнергии из систем городского водоотведения
- Применение звукового датчика уровня жидкости для людей с ограниченными возможностями
- Система автоматизации наружного освещения
- Термоладонь – прибор автоматического измерения температуры тела на входе в учреждение
- «Умный» свет
- Система автоматического открывания крышки и контроль заполнения урны для мусора
- Генератор дома. Двигатель Стирлинга
- Создание Портативного Автоматического Бесконтактного Измерителя Температуры (ПАБИТ-20)
- Разработка экзоруки
- Разработка мобильной игры «ХимикУМ»
- Волонтёрская команда «Тим-ка»
- Автоматизированная парковка
- Создание сельскохозяйственного квадрокоптера «Агро 500»
- Разработка интерактивного сайта для подготовки к олимпиадам по математике
- Создание сайта с нейросетью «CatMe»
- Программа «MY SMART BUDGET» для контроля личного бюджета
- Разработка программного обеспечения для построения трассы искусственного спутника Земли
- Rogmathia – компьютерная roguelike-игра для изучения точных наук в развлекательной форме
- Безопасный обмен сообщениями: мессенджер с шифрованием
- Автоматизированная система дезинфекции воздуха, бесконтактного измерения температуры и обработки рук для образовательных организаций
- Разработка чат-бота для подготовки к ЕГЭ по профильной математике
- Информационный портал «Мир стереометрии»
- Благотворительность online
- Спортивные объекты ЮАО Москвы (Волейбол)
- Создание игры на Unity
- Разработка лидара без движущихся частей под ROS для улучшения алгоритмов движения БПЛА в замкнутом пространстве
- Карта в дополненной реальности
- Умная таблетница с функциями индикации времени приёма таблеток и звукового оповещения
- Медицинский многофункциональный универсальный матрас (эффективный, в том числе для больных COVID-19)
- Шкатулка с кодовым замком
- AR-технологии в школьных учебниках и книгах
- KEINN ONE:1 беспилотный электромобиль
- Бактериальный биореактор
- Повторяшка – тренажер для развития памяти и внимания для самых маленьких
- Мобильное приложение для распознавания Е-добавок eFinder
- Проектирование мобильного интернет-справочника «КакВыжить»
- Модель автоматической системы «Безопасное жильё»
- Чат-бот «Библиотека Ньютона»
- Разработка кроссплатформенной интеллектуальной обучающей игры «АБВГДейка» для привития учащимся начальной школы знаний, понятий и навыков в сфере правописания
- Создание мобильного приложения «Пятиминутка: тренажёр по физике» для платформы Android
- 3D-модель манекена с изменяемыми параметрами
- Стенд для ниток DorTak
- Централизованная, масштабируемая, кроссплатформенная и многопользовательская система "Интернет вещей"
- FedChat: чат с асимметричным шифрованием
- Создание информационного портала для новичков и любителей горных лыж – Properski.ru
- Учебно-игровое пособие «Искатель»
- Автоматический дозатор лекарств
- Настольная развивающая игра «Контур»
- Школа будущего. Современный кабинет математики
- Модель многофункциональной инновационной школы
- Классификация звёзд на языке программирования Python
- Синтез и исследование противогрибковых свойств наночастиц ZnO с этосомным покрытием
- Шифрование файлов на Python гибридным протоколом
- Создание мобильного приложения для помощи в ведении домашнего хозяйства
- Виртуальный музей
- Модель межпланетного космического корабля с оптимальным двигателем
- Моделирование коллекции наград Великой Отечественной войны
- Использование 3D-моделей для создания спортивных аксессуаров
- Создание 3D-модели рукоятки для классического спортивного (олимпийского) лука
- 3D-модель электровиолончели по индивидуальному дизайну
- Кубические иллюзии
- Создание 3D-модели автомобиля для изучения аэродинамических характеристик с использованием программ Autodesk Fusion 360 и SolidWorks 2020
- Наушники для слабослышащих с использованием технологий 3D-моделирования и печати
- Технологии дополненной реальности на службе у музея космонавтики
- Методы получения новых материалов на основе пероксидных соединений олова
- «Арка Шухова»: разработка конструкции по мотивам инженерных решений В. Г. Шухова
- Новый полимерный материал и катализатор для его получения
- Исследование норм потребления средств для стирки
- Чат-бот для решения задач по физике по теме «Кинематика»
- Средство улучшенного распределения контейнеризации в облаке In.Cloud
- Создание трёхмерной модели рельефа (Крым)
- Приложение «Voice». Голос каждого будет услышан
- Создание 3D-модели жилого дома и программы расчёта материалов для его строительства
- Онлайн-мониторинг состояния домашних питомцев по параметрам физической активности
- Система дистанционного контроля обеспечения питьевого режима в школьном корпусе
- Анатомическая накладка на автомобильное сиденье
- Определение применимости лазерных и аддитивных технологий при изготовлении музыкальных инструментов
- Пресс для утилизации алюминиевых банок с пневмоприводом
- ПДД VR
- Приложение для Android по изучению неправильных глаголов английского языка
- Синтез гликопроизводного 1-аминокси-3-аминопропана как потенциального противоопухолевого препарата
- Бифункциональные платформы на основе производных дифенилфосфина для синтеза комплексов золота(I)
- Сравнение бактерий кисломолочных продуктов с пробиотиками, содержащимися в лекарственных препаратах
- Биметаллические тиоцианатные комплексы лантана: синтез и свойства
- Синтез гетерогенного катализатора для селективного получения альдегидов С5
- Усилитель мобильного интернета
- Создание автоматической системы капельного орошения для комнатных растений
- Создание прототипа портативной дозарядочной станции для магазинов автоматических винтовок
- Ионолёт
- Зарядная станция на базе Элемента Пельтье
- Прототип промышленного робота-манипулятора
- Металлополиуретановый гусеничный движитель транспортёра для перемещения тяжеловесных грузов по лестничным маршам
- Рибофлавин: качественный и количественный анализ препаратов и продуктов питания. Измерение спектра поглощения вещества
- Получение наночастиц серебра и их влияние на структуру мезофаз жидкокристаллических алкилоксибензойных кислот
- Сравнительный анализ антибактериальной активности ряда пряных растений (аира, куркумы и имбиря) и оценка перспектив их использования в медицине
- Очистка диглицерида – структурного компонента противоопухолевых катионных глицеролипидов
- Спектральный анализ
- Исследование защитных свойств линз солнцезащитных очков от ультрафиолетового излучения
- Изучение влажности воздуха вблизи различных объектов
- Лазерная бас-гитара
- Эволюционная трансформация лобзика
- Система позиционирования
- Аналоговый и Hi-Fi усилители. Сравнение и анализ характеристик
- Многофункциональная погодная станция
- Трансформатор Тесла. Беспроводная передача электричества и использование резонансных электромагнитных стоячих волн в катушках
- Модульные конвейерные линии
- Транспортная система мегаполиса на примере возможного решения проблем сообщения Москвы и близлежащего города Подмосковья – Видное
- Мини-станция по сортировке строительного мусора
- Модуль для поиска решения задачи N×N в теории игр
- Аэродинамическая труба для моделей
- Разработка онлайн-платформы по бартерным обменам на основе технологии смарт-контрактов
- Основная мысль текста
- Проектирование элементов городского электротранспорта. Электромотоцикл
- Разработка чат-бота «Ромашка»
- Решение базовых задач по физике на термодинамику с помощью программы на платформе PascalABC.net
- Применение технологии блокчейн для продвинутого отслеживания посылок
- База данных олимпиадных и усложнённых задач по точным наукам
- Применение технологии Blockchain для отслеживания состояния пациента
- Онлайн-библиотека для студентов и школьников
- Разработка и внедрение в производство полимерных упругих шарниров, применяемых для аппаратов на коленный и локтевой суставы для детей с нарушениями опорно-двигательного аппарата (в том числе и при ДЦП)
- Светодиодный журнальный стол
- Мультиполигон
- Электронная библиотека для школьных читателей
- Разработка С-компилятора для 16-разрядной виртуальной машины
- Интерактивный сайт, посвящённый волейболу
- Разработка модели инновационной парты
- Дизайн внутреннего дворика корпуса МИРЭА
- Разработка виртуальной кухни с использованием технологий виртуальной реальности
- Лазерный станок с числовым управлением
- Интегрирование сушильной камеры филамента в 3D-принтер Picaso Designer X Pro
- PowerWords: приложение для изучения сложных тем английского языка
- Дизайн внутреннего дворика корпуса В МИРЭА
- Проект моста для пешеходов и велосипедного транспорта в центре Копенгагена
- Стол-трансформер
- Дизайн-проект школы искусств
- «Азбука Шухова «SET OF 33»
- Учебно-познавательная тропа «Ландшафты родного края»
- Игрушка «Детская площадка»
- Специальное рабочее место
- Применение 3D-технологий для визуализации образовательного процесса на примере шахмат и математических фигур
- Разработка 3D-модели Золотого моста
- Виртуально-реальный или комбинированный музей
- Концепция Smart@EPower – социальная сеть потребителей электроэнергии в «Умном городе»
- Синтез ацетона из изопропанола
- Создание автономной энергетической установки с использованием полупроводникового элемента
- Исследование влияния кофеина на рост и развитие бактерий
- Выбор оптимальной схемы армирования и технологии изготовления деталей беспилотного летательного аппарата из композиционных материалов
- Автоматизированный поворотный предметный столик для поляризационного микроскопа
- Система безопасности «Чистый воздух»
- ReКуп
- Постройка судна на беспилотном управлении
- Аэротакси
- Муниципальный многофункциональный робот
- Реновация школ серии МЮ
- Ячейки для хранения личных вещей
- Лазерные технологии в современной школе
- Разработка модели подвижного медицинского комплекса на базе трансформируемого полуприцепа
- Разработка айдентики детского клуба спортивных танцев Let's Dance
- Дизайн, архитектура и современные технологии. Трансформация: арт-объект – VR-музей
- Организация мероприятий по ресурсосбережению
- Разработка интеллектуализированной системы поддержки принятия решений обеспечения безопасности NannyNet
- Игровой алгоритмический тренажёр для младших школьников – робот «Шагайка»
- Регулирование освещённости в комнате с помощью фоторезистора и потенциометра
- Интеллектуальная система управления оконными жалюзи
- Карманный кардиомонитор
- Изучение эффективности антибактериальных медицинских средств
- Решение задачи о брахистохроне опытным путём
- Автоматическая кормушка для кота
- Изучение антибиотических свойств препарата «Ротокан» и его компонентов
- Создание простых механизмов на основе принципов гидравлики
- Разработка упрощённой схемы определения допинга в лекарственных препаратах
- Получение обратной эмульсии с инкапсулированным ниацинамидом
- Синтез бутаналя и его анализ
- Разработка нового композитного материала для использования в авиастроении
- Идентификация и количественное определение 6-аминокапроновой кислоты в лекарственных препаратах
- Разработка упаковки пищевых продуктов для пролонгации их сроков хранения
- Влияние легирующих элементов и термической обработки на структуру и свойства сплавов на основе алюминия, используемых в промышленности
- Агенты для фотодинамической терапии на основе металлоорганических соединений
- Определение критической температуры диоксида углерода методом электронного парамагнитного резонанса
- Исследование эксплуатационных свойств фильтрующих картриджей
- Металл-полимерные композитные мембраны для выделения водорода из газовых смесей
- Микробный топливный элемент
- Получение экстракта слизи улиток и его использование для внеклеточного матрикса
- Синтез аденинового мономера пептидно-нуклеиновых кислот на основе L-глутаминовой кислоты с циклогексильной защитой и оценки его выхода
- Нелинейно-оптические лимитеры для защиты органов зрения от высокомощного лазерного излучения
- Проектирование и разработка бионического протеза ноги
- Сравнение эффективности катушек индуктивности разных форм для беспроводной передачи энергии имплантируемым медицинским устройствам
- Создание 3D-модели школы
- Гроубокс
- Приложение для обучения правилам дорожного движения (ПДД)
- Разработка виртуального тренажёра для развития навыков вождения автомобиля с использованием технологий виртуальной реальности
- Induction Heater / Индукционный нагреватель
- Robotic Hand Роботизированная рука
- Master Bin 20.2.0: a Smart Waste Collection and Sorting System / Интеллектуальная система сбора и сортировки использованной тары «Master Bin 20.2.0»
- Сигнализация
- Разработка прототипа серийной модели светоуправляемой колесной платформы
- Прибор для контроля уровня pH водной среды в аквапонической установке
- Прототип энергоэффективного индикатора на микроконтроллере ESP32 и полевых транзисторах
- Создание устройства для исследования подводных источников газа (сипов)
- Использование лазера для измерения концентрации взвешенных частиц в воздухе
- Умное медицинское устройство (УМУ) для предварительной постановки диагноза с применением микроконтроллера Arduino
- Световой будильник
- Мультифункциональный шлюз управления
- Создание манипулятора с цветовой идентификацией предмета
- 3D-«крестики-нолики» на Arduino
- Многофункциональная роботизированная станция для занятий рисованием
- Прибор для измерения электромагнитного излучения в быту
- Столик с электронным управлением для фотографирования минералов
- Регулирование влажности воздуха в комнате
- Устройство зарядки с элементом Пельтье
- Проектирование корпуса для обучающей интерактивной карты звёздного неба
- Создание конструкции пульсирующего сердца при помощи микроконтроллера ATtiny2313
- Создание теплицы с автоматическим поливом растений
- Исследование зависимости передаточных и выходных характеристик полевых транзисторов на основе органических кристаллов-полупроводников DH-P-TTA от материала электродов
- CMC (Clever Morning Closet)
- Браслет управления автомобилем
- Современная копилка
- Спасательный маячок
- Электронный арбитр для интеллектуальных игр
- Аппаратно-программный комплекс термомеханической сборки печатных плат
- Прототип пожарной сигнализации
- Ошейник, облегчающий поиск потерявшегося животного
- Разработка периферийного устройства, которое будет предупреждать появление проблем со зрением при роботе с компьютером
- Музыкальная катушка Тесла
- Проектирование и моделирование светодиодных созвездий
- Индуктивный датчик для измерения импульсных токов с амплитудными значениями порядка 1-2кА
- Автоматическая теплица для выращивания специй
- «Умный» зонт
- Сортировка пластика
- Полуавтономная солнечная панель
- Автоматизация кастрюли
- Разработка и создание программируемого робота, дозирующего и раздающего жидкости
- Портативная сигнализация для кошельков и телефонов
- Создание автоматизированной технологической домашней теплицы
- Кроссплатформенный проигрыватель на Python
- Беспилотный шнекоход
- Канатная дорога как промышленный транспорт в условиях Луны
- Изготовление прототипа катера с ДВС
- Разработка концепта транспортного средства для исследования Арктических зон
- Эндуро мотоцикл
- Гусеничная платформа высокой проходимости
- Влияние резонатора на работу двухтактного двигателя
- Бионический квадрокоптер "nonopus"
- Разработка и создание автоматизированного робота для сортировки мусора
- Навигатор по вузам Москвы
- «Linkage»
- Система оповещения о лесных пожарах
- Приюты для животных
- Методы реализации устройств «умного» дома
- Прогнозирование технологических параметров процессов установки первичной переработки нефти с использованием современных программных средств нейросетевого моделирования (Deductor Studio Academic)
- Программа на языке Python для создания трасс по классической скорости в спортивном скалолазании
- Разработка мессенджера для школьной коммуникации
- Новое применение RFID- технологии в метро
- Разработка приложения дополненной реальности для музея
- Разработка сайта о ветеранах Великой Отечественной войны
- Визуализатор G-кода
- Программа для автоматизации работы с интерфейсом персонального компьютера
- Индивидуальный подбор технических олимпиад для учащихся 8–11 классов
- Универсальный модуль для космических исследований
- Определение колеи и базы автотранспортного средства в криминалистике
- Создание ассистивного устройства для слепых и слабовидящих людей
- Компьютерная система обобщающей обработки результатов тестирования
- IoT-control of the indoor plants and their watering / IoT-контроль и полив комнатных растений
- Устройство помощи в ориентировании слабовидящих людей
- Разработка сайта приюта для домашних животных
- Централизованная сеть для удалённого коллективного ведения базы данных домашних заданий школьника
- Разработка сайта-энциклопедии по математике
- Конструирование плоттера
- Идентификация личности по цветовому ключу при помощи камеры
- Применение технологий «блокчейн» в сфере оказания услуг горнолыжных комплексов
- Методы симметричного шифрования
- Разработка сервиса автоматического сбора, фильтрации и анализа новостей о ДТП, произошедших в РФ
- Реализация алгоритма PageRank и его тестирование на реальных данных
- Разработка рекомендательной системы по подбору музыки
- Многофункциональная система шифрования «MES»
- Мобильное приложение AutoTourist
- Создание макета трансформируемого модуля космической станции
- Сравнение методов аппроксимации данных путём минимизации функций невязки различных видов
- Создание приложения, предназначенного для нахождения мест по утилизации мусора
- Инструментальная платформа для разработки специализированных вычислительных систем
- Разработка расширения для браузера, основанного на системе Blockchain, в целях решения проблем безопасности хранения своих и чужих паролей и аккаунтов в интернете
- Мобильное приложение голосовой помощник «ЧАЙКА»
- Игра «WIRES», обучающая основам алгоритмизации
- Развивающее приложение для детей «Умножайка»
- Конструкция «Вертикальный сад» с автоматизированным поливом для поддержания экологии школьной среды
- Чат-бот для решения квадратных уравнений
- Генеративное проектирование робота-манипулятора
- Разработка математического интернет-тренажёра по устному счёту
- Создание интерактивного квеста «The FORTune of ROSS» как ключевого мотивационного инструмента в изучении истории и культуры России и США
- Создание нейронной сети для определения состояния сна человека
- Онлайн-платформа MathBattle
- Программа – визуализатор силовых линий поля
- Система автоматизированного контроля соблюдения питьевого режима
- Система визуализации и контроля передвижения
- Создание игры-тренажёра для решения задач физико-математического цикла
- Автоматизация подготовки заготовок печатных плат
- Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой: синтез и применение
- Подбор оптимального флюорофора для использования в нейрохирургии с флуоресцентной интраоперационной визуализацией
- Синтез субклеточно-нацеленных фотосенстибилизаторов
- Разработка состава и технологии получения шипучей таблетки с экстрактом черники
- Разработка аналогового действующего вещества препаратов для лечения и профилактики железодефицитной анемии
- Синтез двойных ортофосфатов и ортованадатов гадолиния и исследование их свойств
- Наноматериал для улучшения качества родниковой воды
- Оптимизация методов выделения бактериопурпуринов
- Миметик глицина на основе производного гераниола
- Military drone – «Shooter»
- Новая аэродинамическая компоновка летательного аппарата
- Ультразвуковой контроль скорости внутренней коррозии стальных ёмкостей и трубопроводов
- Исследование электромагнитной индукции на примере создания металлодетектора
- Адаптивная система экономии электроэнергии
- Применение современных датчиков и средств сбора данных при демонстрации физических законов
- Винт вертолета из углепластика
- Система позиционирования и навигации для «Умного города»
- Исследование бумаги А4 на прочность
- Зонд для сбора данных о явлении пробоя на убегающих электронах
- Исследование и инновационное практическое применение сплава с эффектом памяти формы
- Синтез липида-хелпера – компонента катионных липосом для генной терапии
- Создание косметических средств на основе экстракта алоэ вера и на основе аллантоина
- Создание флуоресцентного зонда для изучения метаболизма метформина
- Синтез и подбор оптимальных условий очистки Sn-комплексов лизина
- Выбор растворителей для реакции получения эпихлоргидрина на основе исследования их свойств
- Индикатор срока годности
- Исследование примесей в составе зарубежного препарата и его российского аналога
- Синтез аналога радиофармпрепаратов на основе металла галлия и хелатора тетракарбоновой кислоты (DOTA) с потенциальной визуализирующей и противоопухолевой активностью
- Влияние буферных агентов на процесс меднения
- Оптимизация процессов синтеза комплекса гадопентетовой кислоты, используемого в качестве контрастного диагностического препарата для магнитно-резонансной томографии
- Сорбционная очистка сточных вод гальванического производства от смесей тяжёлых металлов и органических компонентов
- Разработка джема с добавлением хлорофилла
- Разработка сорбента для аффинной хроматографии на основе пептидомиметиков
- Получение натурального корригента запаха для дезинфектанта в форме спрея
- Суперконденсатор и области его применения
- Разработка программного решения для определения угла поворота магнитометра
- Изучение природных фотонных кристаллов методами современной микроскопии
- Исследование влияния вакуума на процессы преобразования веществ
- Исследование предельных характеристик MEMS-гироскопа в реальных условиях для осуществления задач навигации и стабилизации объектов в пространстве
- Технико-экономическая оптимизация параметров бытового воздухоочистителя
- Система синхронизации на основе механического модулятора оптического сигнала
- Визуализация магнитного поля
- Трансформатор Теслы как атрибут школьной лаборатории, наглядно демонстрирующий свойства электрического тока
- Исследование длительного переохлаждения водных суспензий, запертых под углеводородной плёнкой
- Водный исследовательский комплекс «ВИК-2»
- Создание модели имплантируемого кардиостимулятора с беспроводным энергообеспечением
- Эффективность дезинфицирующих средств бытовой химии
- Инкубатор для эксперимента
- Проектирование и разработка автоматизированной системы отслеживания состояния людей с сердечно-сосудистыми заболеваниями на основе дистанционного измерения ритма сердца
- Создание осязаемой 3D-реконструкции Третьего Кавалерского корпуса Царицынского дворцово-паркового ансамбля
- Система контроля воды в кулерах
- Система помощи при эвакуации
- Комплексная система безопасности мотоцикла
- Фотонная структура для управления электромагнитным излучением
- Возможности бесконтактной передачи вращения
- Разработка прототипа мобильной роботизированной платформы для помощи в сельском хозяйстве «Siberian tiger»
- Сонификация сложных физических процессов как средство отображения информации в тифлопедагогике
- Определение ионного состава водных растворов с помощью лазерной спектроскопии комбинационного рассеяния и метода искусственных нейронных сетей
- Создание онлайн-музея «Великая Победа»
- Психоэмоциональный тренажёр, восстанавливающий мимику у людей, перенёсших инсульт
- Мобильное приложение «Дневник самоконтроля»
- Проектирование мобильного интернет-справочника «КакВыжить»
- Интеллектуальная игра
- Обработка изображений с помощью языка программирования Python 3.7
- Проектирование размещения мебели в дополненной реальности
- Разработка приложения с использованием дополненной реальности для визуализации приготовления блюда по заданному рецепту
- Приложение дополненной реальности для визуализации географических карт
- Приложение дополненной реальности для визуализации содержания ячеек хранения систем складского учёта
- Метеостанция
- Улучшение работы системы светофоров на перекрёстке
- Глубокая модернизация 3D-принтера Cubex trio компании 3DSystems
- Интеллектуальная система дистанционного полива комнатных растений
- Система автоматизированного учёта сбора пластиковых крышечек
- Автоматизация грибной фермы
- Разработка «умного» коврика на Arduino
- Stereomix
- Робот на самоуправлении
- Шаг на пути к антропоморфным роботам
- Проблема загрязнения окружающей среды бытовыми отходами. Моделирование удобной «корзины» для раздельного сбора мусора
- Разработка мобильной платформы под управлением голосового интерфейса для осуществления работ в труднодоступных местах
- Детская площадка в стиле Minecraft
- Устройство мониторинга местности
- Дистанционно управляемый мобильный робот общего назначения (ДУМРОН)
- Исследование погрешностей в работе квадрокоптера в разностно-дальномерном режиме позиционирования TDoA2
- Робот удалённого присутствия
- Акцентирующее освещение в сценографии
- Макет «Высота «Погранзнак»
- Робот-кошка
- Радиоуправляемое судно для очистки водоёмов
- BIM-технологии в строительстве
- Выявление методов нейтрализации несанкционированных беспилотных летательных аппаратов
- Практическое применение компьютерного зрения
- Проект «Арт-объекты в стиле графики А. С. Пушкина "У Лукоморья"»
- Пилотируемый трикоптер TRIFLY, выполненный из сверхлёгких композиционных материалов
- Дизайн универсальной деки для лонгборда BAUBOARD, выполненной из сверхлёгких композиционных материалов
- Создание мини-трактора
- Разработка и конструирование двигателя внутреннего сгорания с использованием 3D-принтера
- Сценография. Создание декораций к школьному спектаклю «Король Лев»
- Применение суспензии тонкомолотого перлита для повышения прочности цементного камня
- Программа строительства оптимального по цене частного дома
- Лодка из композитных материалов
- Диодно-лазерный станок
- «Умный» светильник
- Создание элемента интерьера с помощью средств цифрового производства
- Хранение медикаментов для людей с хроническими заболеваниями
- GreenBox («умная» теплица)
- Робот для автоматизированной сортировки мусора
- Образовательное приложение с дополненной реальностью «Interactive road signs»
- Виртуальная химическая лаборатория
- Нейронная сеть. Умный староста
- Использование панелей в качестве альтернативного источника энергии в школе
- Распознавание лиц в школе
- Приложение-энциклопедия экзотических фруктов
- Создание 3D-модели радиатора и её применение в процессе изготовления пульта проверки
- Гидроэлектростанция турбинного типа
- «Радиопломба» – цифровое устройство, ликвидирующее хищения электроэнергии
- Конструирование деталей и проектирование электронной схемы ветроэлектрогенератора
- Образовательный стенд «Бионический протез»
- Экскурсионный 3D-маршрут по корпусу института тонких химических технологий Российского технологического университета МИРЭА с использованием VR-технологии
- Разработка тактильной карты для слабовидящих детей
- Флейта из углепластика
- Проект визуализации рассказа Р. Бредбери «Всё лето в один день» с использованием технологий виртуальной реальности
- Моделирование: ферментация чеснока в домашних условиях
- Разработка и создание прототипа устройства, помогающего людям с дефектами зрения определять сигнал светофора
- Мышка для людей с ограниченной подвижностью рук
- Устройство для мониторинга температуры тела у животных
- Автоматическая система управления светом (АСУС)
- Химия – просто! История создания одной компьютерной игры
- Робот-экскурсовод
- Модель бьющегося сердца
- «Умная» система пневмоочистки IT-устройств
- Разработка смарт-контракта для осуществления торговых сделок
- Приложение для детей младшего и среднего школьного возраста «Звук и Слово»
- Устройство контроля уровня мусора в контейнере
- Автоматизированное освещение в непроходных помещениях
- «Компьютерное зрение». Система доступа на объект посредством распознавания лица
- Проектирование персонального 3D-принтера
- Создание декораций для спектакля на основе чертежей, рисунков, 3D-моделирования по повести-сказке Эрнеста Теодора Амадея Гофмана «Щелкунчик и Мышиный король»
- Использование VR-технологий при проектировании городского парка
- Разработка виртуального проекта будущей квартиры с использованием технологий виртуальной реальности
- Архитектурная визуализация и VR-технологии
- Мобильное приложение «Школьная лаборатория в дополненной реальности»
- Инновационный кабинет информатики
- «Мы смотрим на звёзды, или звёзды смотрят на нас?»
- Разработка образовательного приложения по географии с использованием AR-технологий для инклюзивного образования
- Приложения дополненной реальности для образования
- Арт-объекты на Arduino для площадок Москвы
- Макет ветрогенератора с вертикальной осью
- Архитектура метаболизма. Модульные системы
- Невероятная эволюция изоморфов (применение генетических алгоритмов в программировании)
- Разработка компьютерной игры Cube Rush в Unity
- Программа для шифрования «Securnote» (информационная безопасность)
- Робот «ГОР» для дистанционного осуществления погрузочно-разгрузочных работ
- Разработка метода выделения белка из растительных продуктов
- Разработка и создание приложения для калибровки камеры под квадрокоптер «Клевер»
- Разработка метода выделения пектина и фуранокумаринов из борщевика Сосновского
- Создание сопел жидкостных ракетных двигателей
- «Умная» теплица
- Получение поликатионного амфифила для создания липосомальных структур в генной терапии
- Создание системы доставки лекарств на основе магнитных наночастиц
- Разработка автономного беспилотного летательного аппарата без использования систем GPS и ГЛОНАСС
- Система распознавания лиц в школе
- Средство передвижения для людей с ограниченными возможностями с функцией мониторинга сердечно-сосудистой системы и дистанционным управлением
- Создание виртуальной экскурсии по Музею истории вычислительной техники в «Школе № 1530 «Школа Ломоносова»
- Автоматизированное управление микроклиматом теплицы для выращивания редких экзотических и лечебных растений
- Создание приложения под Windows для управления PTZ-камерой
- Игра как эффективный метод изучения Красной книги Московской области
- Разработка электронного устройства «Умный турник» на основе Arduino
- Разработка лабораторного стенда для исследования ПИД-регулятора
- Умное стекло
- Автоматизация технологического процесса подготовки заготовок печатных плат
- Управляемый комплекс для имитации дневного освещения аквариума
- Разработка и постройка БПЛА мультироторного типа для нанесения граффити на вертикальные поверхности
- Создание системы распознавания заболеваний растений с использованием машинного зрения и БПЛА
- Внедрение магнитной левитации в подвеску автомобиля
- 3D-расчёты магнитной системы
- Разработка сервиса для организации поисково-спасательных операций Rescue Map
- Изучение влияния антимикробных пептидов на антибиотики при их совместном применении
- Модель робота-сортировщика
- Устройство для кипячения воды, работающее через USB на эффекте Пельтье
- Создание мембраны для актуатора
- Методический конструктор для слепых и слабовидящих детей «Сириус»
- Создание и исследование коронно-разрядного двигателя
- Универсальная автономная установка генерирования электроэнергии
- Робототехнические системы в современных технологиях
- Создание интернет-ресурса «Здоровый сон»
- Увлекательная система сбора использованных батареек
- Использование солнечных панелей в качестве альтернативного источника энергии в школе
- Модель-конструктор к урокам биологии в школе «Сравнение растительной и животной клеток»
- Определение подлинности лекарственных средств на Российском рынке фармацевтики на примере района Куркино
- Электровелосипед
- ARmuseum
- Взаимодействие жидкокристаллических алкилоксибензойных кислот с растворителями
- Фотокатализаторы на основе диоксида титана: получение и применение
- Комплексные соединения РЗЭ с фосфоновыми кислотами: синтез и их применение
- Технология дополненной реальности AR в образовании «Растительная и животная клетка»
- Разработка облучательной установки для повышения продуктивности процесса фотосинтеза
- Метаматериалы
- Быстрее ветра, или Может ли исследование сопротивления воздуха помочь создать модель нового транспортного средства
- Светодиодный куб 8˟8˟8
- Наглядное пособие для демонстрации явления самоиндукции
- Мобильная робототехническая система для трёхмерного сканирования
- Модификация алюминиевого сплава АД0 путём придания его поверхности супергидрофобных свойств
- Синтез и выделение ароматизаторов. Исследование возможности их применения при изготовлении мыла
- Сокращение тепловых потерь в системе ХВС и ГВС
- УФ-очистка воды
- Ультразвук и его влияние на живые организмы на примере дрожжевых клеток
- Разработка супергидрофобных покрытий на поверхности магниевого сплава МА8
- Связывание катионных препаратов с различными биологическими лигандами
- Влияние выбора растворителя на продукт взаимодействия цинка с йодом
- Функционирующая модель модуля космической станции с радиоуправляемыми бортовыми системами жизнеобеспечения
- Беспроводная Bluetooth-колонка с автономным источником питания
- Медицинский тренажёр-симулятор для обучения мануальным навыкам эндовидеохирургии
- Интерактивный программируемый театр
- Разработка технологии получения биоразлагаемых амфифильных блок-сополимеров
- Автоматическая кормушка для питомца
- Умная бионическая рука
- Энергосберегающая система контроля и управления «Умный дом»
- Мехатронный модуль «Контрольно-сортировочный автомат»
- Металлоискатель
- Модель двигателя Стирлинга
- Ветер: бесплатная энергия вокруг нас
- Декоративный увлажнитель воздуха
- Виброжилет
- Автоматизация полива: качество выше при меньших издержках
- Создание препарата комплексного действия на основе производного хлорофилла
- Моделирование поведения металлосодержащих препаратов для терапии и диагностики рака в человеческой сыворотке
- Интеллектуальный комплекс систем оповещения с применением GSM-модуля
- Система автоматизированного контроля врача-анестезиолога
- Разработка комплекса программного обеспечения для образовательных организаций
- Нейротехнологии и высокотехнологичные протезы. Установка для изучения мозговых сигналов и мышечных реакций
- Иммобилизованный фотопереключаемый флуоресцентный белок как основа для носителя информации
- Стенд-скоростемер (универсальный разгонный стенд для измерения скорости кордовых моделей автомобилей)
- Электростатический напылитель
- «Разработка устройства для быстрой очистки школьной доски «FastClean»
- Создание защиты из композитных материалов
- Исследование физико-химических свойств смеси ацетонитрил – циклогексанон и оценка возможности её разделения с использованием ректификации
- Ультразвуковой метод ориентации в пространстве с применением компьютерного зрения для слепых и слабовидящих людей
- Автоматическая линия производства вязких лекарственных препаратов
- Разработка тренажера реакции
- Система для терморегулирования одежды рабочих в условиях Крайнего Севера
- Программируемый аудиозамо́к
- Макет 1 : 87
- Умный увлажнитель воздуха
- Система автоматизированной оценки качества водительских навыков
- Разработка программного обеспечения системы автоматического управления конвейерами машин типа СЗ
- Умный рюкзак (Smart backpack)
- Воздействие лазера постоянного излучения с длиной волны 532 нм на старую бумагу
- Система мониторинга нарушений ПДД детьми и подростками
- Многофункциональный контейнер для перевозки растений
- Персональный летательный аппарат
- Переработка пластиковых отходов в условиях малого бизнеса
- Инновационный вид транспорта, представляющий собой гибрид монорельса и канатной дороги
- Разработка модели автоматической системы обеспечения непотопляемости корабля
- Разработка концепта транспортного средства для исследования арктических зон
- Разработка базового модуля сети контроля окружающей среды
- Устройство борьбы с засыпанием водителей «Антисон» в процессе вождения
- Модульная многофункциональная космическая система
- Системы рекуперации в гибридном автомобиле
- Авторотация как эффективный способ спасения метеорологических ракет
- Разработка станка для заточки вольфрамовых игл
- Создание прибора для определения параметров микроклимата
- Техническое средство робот PinGo для реабилитации детей с ограниченными возможностями
- Макет инновационной школьной парты
- Создание живых обоев на окнах
- Дизайн-проект IT-полигона на базе ГБОУ Школы № 1532
- Метод оценки устойчивости склонов заданного участка местности
- Программно-аппаратный комплекс предупреждения возникновения пожаров на открытом пространстве
- Робот, собирающий кубик Рубика
- Космическая станция
- Карданов подвес с электроприводом, дистанционным управлением и компьютерной визуализацией положения макета в пространстве
- Полётный контроллер для мультироторных систем
- Модель устройства помощи при экстренном торможении
- Модель радио А.С. Попова на уроках физики и во внеурочной деятельности
- Магнитный бестопливный генератор энергии
- Волновой маятник: разработка компьютерной и механической модели маятника Чеботаева
- Мини-гидроэлектростанция для многоквартирного дома
- Судно на воздушной подушке для очистки водоёмов
- Моделирование переноса пластиковых объектов в вихревых течениях
- Автономный конденсатор − накопитель воды, работающий на принципах законов физики в условиях жарких засушливых регионов
- Исследование влияния топологии подложки на формирование и рост островковых тонких плёнок меди
- SmartTBox
- Универсальный робот-транспортёр
- Беспилотное транспортное средство
- Добыча электроэнергии из воды
- Исследование и визуализация точки бифуркации
- Перспективы золотоносности Сочинского района. Научные разработки диагностики минерального состава сульфидных руд
- Эффективность ветрогенераторов с различными конструкциями роторов
- Применение высокодетальных данных спутниковой съёмки для предотвращения гибели гренландских тюленей в акватории Белого моря
- Электронный живописец
- Робот - «трубочист»
- Согревающий жилет на химических источниках тепла
- Изготовление деталей для станка UNIMAT
- Разработка прикладного программного обеспечения для тестирования экспериментальных структур сверхпроводник-изолятор-сверхпроводник (SIS-переходов)
- Мобильная система видеосъемки «Паук»
- Протезирование точной копии кисти руки человека на основе результатов трёхмерного сканирования
- Тактильные лабиринты Москвы
- Визуализация школьной формы в электронном формате
- Гидрологический цикл
- Разработка и создание лазера на молекулярном азоте с поперечным разрядом
- Ионофон − «поющая» плазма
- Моделирование и анализ развития градостроительного планирования территории мегаполиса с помощью технологий виртуальной реальности и космического мониторинга
- Симулятор «Пожарный»
- SmartCage. «Умная» клетка для домашних грызунов
- «Умная» крыша» с использованием альтернативных источников энергии и применением микроконтроллера ARDUINO IDE
- Универсальная химическая 3D-модель молекулы и атома
- Симулятор «Граффити»
- Нейронная сеть для обнаружения DGA
- Разработка Android-приложения для автоматизированной проверки устной части ЕГЭ по английскому
- Тактильный набор для построения блок-схем алгоритмов
- Создание мобильного ANDROID-приложения для дистанционного управления роботом входящего в базовый комплект образовательного робототехнического модуля «ТЕХНОЛАБ – базовый уровень»
- Разработка компьютерной игры «LONER» на Unity
- Применение технологии Blockchain для оптимизации работы баз данных спортсменов
- Построение сети организации или маленького офиса
- Telegram news bot на «Python»
- Модульное покрытие-трансформер
- Разработка ботов при помощи Discord API
- Игра для развития устного счёта
- Разработка программно-аппаратного комплекса по отслеживанию посещения учащихся
- «Умная» теплица
- Применение технологии Блокчейн в сфере предоставления гарантий на товары
- Создание интернет-ресурса «Городские квесты»
- Система контроля безопасного для зрения детей использования компьютера
- Управление ВЧ-генератором с помощью программных средств LabVIEW
- Онлайн чат-бот
- Создание химического калькулятора
- Мобильное приложение «Weather Assistant»
- Интернет-ресурс «РУКА ПОМОЩИ» для начинающих пользователей старшего поколения
- Компьютерная программа в виде игры для обучения будущих программистов
- Модульная платформа для разработки высокопроизводительных встраиваемых систем на базе программируемых логических интегральных схем
- Создание интерактивного квеста по химии
- Применение технологии 3D-моделирования в реальной жизни
- Свёрточные нейронные сети для распознавания дорожных знаков
- Knowledge Land – развивающий портал для детей
- Создание игры в GameMaker Studio
- Разработка сети сайтов, посвящённых путешествиям и описанию стран
- Мобильное приложение - словарь и упражнения для изучения английского языка
- Создание интерактивного введения в курс геометрии
- Влияние температуры и природы катализатора на селективность протекания реакции конденсации кетонов
- 3D-принтер
- Искусственный агент с эмоциональной речью и жестами – прототип человекоподобного робота
- Интеллектуальный пульсоксиметр
- Крылья обратной стреловидности
- Мобильное приложение «Автоматизированный контроль состояния здоровья инсулинозависимых людей»
- Единый портал школьных газет Москвы
- Эпоксидирование аллилхлорида
- Альдольная конденсация пропионового альдегида
- Создание роботов для участия в соревнованиях
- Разработка программы автоматизированного составления расписания в школе на основе генетического алгоритма
- Мобильная роботизированная платформа «Siberian Tiger» для помощи в сельском хозяйстве
- «Умная» вентиляция для умной школы
- Система автоматического полива растений
- Физика супертороидов
- Управление роботом при помощи модуля электромиографии (ЭМГ модуля)
- Автоматизированный полив растений
- Симулятор «Крановщик»
- Дополненная реальность в школьном музее «Тайны русского зодчества»
- Математические закономерности в творчестве Никола Пуссена
- Путешествие в мир дополненной нереальности
- Мебель из паллет
- Решение проблем организации сортировки ТБО в зонах жилой многоэтажной застройки
- Разработка и изготовление «Ленинградского» репродуктора 1941 г.
- Проектирование и разработка базы данных крупных торговых центров Москвы
- Разработка веб-сайта для помощи в выборе профессии «wanttobe.pro»
- Разработка потенциальных агентов для комбинированной терапии на основе комплексов олова и природных хлоринов
- Проектирование приложения для обеспечения эффективной и безопасной работы в сети Интернет
- Разработка приложения для навигации по зданию (университета)
- Создание и изучение свойств липофильного диамина с потенциальной противоопухолевой активностью
- Проектирование приложения поддержки планирования и организации осуществления покупок «WishMaker»
- Проектирование приложения музыкального справочника
- Адаптивная система экономии электроэнергии
- Получение производных бактериохлорофилла для биомедицинского применения
- Интерактивный дизайн в виртуальной реальности
- Порфирины – материал для технологии будущего
- Автономные интерактивные информационные стенды на улицах современного мегаполиса
- Создание игры для развития эмоционального интеллекта
- «Вижу свет, или Исследование качества защиты зрения солнцезащитными очками»
- Разработка сайта Московской детской железной дороги
- Модель электромагнитного поезда
- Система оповещения «SOUNDER»
- Модель мобильного лазерно-гравировального станка для выполнения работ на вертикальных поверхностях
- Извлечение соединений неодима из шлифотходов
- Макет школьного лифта
- Компьютерная игра с элементами обучения
- Технология изготовления радиоуправляемого трицикла
- Акустическая колонка своими руками. Выгодно ли собрать ее самому
- Разработка андроида для изучения взаимодействия роботов с людьми
- Влияние структуры фотосенсибилизаторов на связывание с человеческим сывороточным альбумином
- Анализ уровня экспрессии генов VEGF и его рецепторов KDR / FLT-1 методом ОТ/ПЦР в образцах клеточной РНК из биоптатов пациентов с новообразованиями предстательной железы
- Создание 3D-модели-конструктора «Клетка»
- Логическая игра «Перевозчик, Волк, Коза и Капуста»
- Система спасения при пожаре из многоэтажных строений «Лифт жизни»
- Проектирование приспособления для получения различных сферических и фасонных поверхностей на примере фрезера Makita RP2300FC
- Создание прототипа БПЛА
- Морфометрия мозга
- Проектирование и разработка специального программного обеспечения для устройства мониторинга стресса
- Проектирование и разработка действующей модели мобильного ракетного робототехнического комплекса
- Изучение влияния условий запуска и лётных характеристик бумажных самолётиков на дальность их полёта
- Транспортное средство для экстремального вида спорта. Drift-trike. Постройка и модернизация
- Автоматическая система мониторинга учебного помещения на соответствие нормам СанПиН
- Установка для измерения скорости вращения электродвигателя
- Катионные липосомы – эффективные системы доставки лекарственных препаратов нового поколения
- Устройство для автоматизированного изготовления печатных плат путём фрезерования проводящего рисунка
- Модель роботизированного устройства для токарно-фрезерной обработки деталей
- Умный переход («SMART CROSSWALK»)
- Создание аэросаней-амфибии на дистанционном управлении для доставки спасательных средств потерпевшим на воде
- Создание геоинформационного портала средствами QGIS
- Исследование способов оптимизации нейросетевых вычислений
- Формирование наноструктурированных покрытий методом магнетронного распыления
- Эффективный ветрогенератор
- Поиск пути в топографических условиях
- Биметаллические терефталаты лантанидов как люминесцентные термометры
- Concept Art. Artbook. The Age of Snowbounded
- Прототип модульного умного дома
- Выявление и устранение проблем с освещением на больших территориях
- Гидротермальный синтез корунда и его цветных разновидностей
- Ацетофенон как новый стабилизатор пероксида водорода
- Мобильная солнечная электростанция с системой слежения за солнцем
- Изучение условий конусообразования сыпучих тел
- Автоматизированная касса самообслуживания
- Разработка системы дистанционного управления домом на базе платформы Arduino
- Изменение поверхностного рельефа титанового сплава в плазме высокочастотного индукционного разряда
- Мини уборочная машина
- Создание сканирующего туннельного микроскопа
- Автономная исследовательская платформа для изучения физических свойств окружающей среды
- Робототехническая система нанесения дорожной разметки
- Робот по обслуживанию склада
- Робот-собиратель
- Иллюстрированная книга «Каменный гость» по произведению А. С. Пушкина
- Интеллектуальная система обнаружения пожара
- Организация вертикального сада в интерьере школьного пространства
- Разработка агрегата для проверки герметичности упаковки лекарственных препаратов
- Влияние режима сна на развитие тревожности у подростков
- Ножничный подъёмник
- Создание электробайка EFEB
- Проект 3D-модели навигации по зданию аэровокзального комплекса
- Конструирование велосипеда с электроприводом
- Ветрогенератор
- «Зенит» и веб-камера
- Малые архитектурные формы
- Радиоактивные металлы как средство для терапии и диагностики
- Модульная роботизированная техника для уборки промышленных отходов на территории Заполярья и для планового развития региона
- Преобразование «шаговой» энергии в электрическую и использование её для нужд мегаполиса
- Разработка и изготовление набора деталей для 3D-печати, для изучения робототехники
- Генератор альтернативной энергии
- Робот-уборщик
- Протезирование руки
- Исследование химического состава и физических свойств батареек при различных условиях эксплуатации
- Сборка гальванического элемента и повышающего преобразователя и его использование для изучения электролитической диссоциации растворов электролитов
- Катушка Тесла
- Экспресс-метод качественного и количественного определения анальгина в лекарственных препаратах
- Прибор для отслеживания микроклимата в учебных заведениях
- Исследование зависимости изменения выталкивающей силы соляных растворов программно-аппаратными средствами сбора и обработки данных
- Золотое сечение в архитектуре
- Проект системы автоматизированного полива выращиваемых растений (рассады) в закрытых помещениях малых площадей
- Создание WEB-приложения «Электронный библиотекарь» с функцией генерации и обработки штрих-кодов и инвентаризацией склада
- Программный расчет количества и цены пиломатериалов для возведения малометражной одноэтажной постройки с односкатной крышей
- Умный дом: новейшие технологии для реальной жизни
- Создание мобильного приложения "MoreGEO"
- Красота может быть экономной
- Робо-шаттл: автоматическое транспортное средство для аэропортов
- Исследование проходимости транспортных роботов
- Использование технологии PBR для VR-визуализации интерьера
- Воздействие электростатического поля на пламя
- Разработка и постройка беспилотного летательного аппарата (БПЛА) самолетного типа для профессионального применения
- Перечисление соответствий между конечными множествами
- Создание действующей модели мотопланера
- Антивирусный сканер InfANT
- Робот-транспортер
- Катушка Тесла
- Применение технологии Blockchain для оптимизации работы баз данных спортсменов