в московской школе
Влияние условий процесса СКФ-микронизации на растворимость моксифлоксацина и левофлоксацина
|
Работа призёра конкурса проектов и исследований «Старт в медицину» открытой городской научно-практической конференции «Старт в медицину» в секции «Биохимия» |
Направление работы: Биохимия
Авторы работы: ГБОУ Школа № 2054
Email: Написать
Предметы: Биология, Химия
Классы: 10 класс
Мероприятия: Конкурс проектов и исследований «Старт в медицину» открытой городской научно-практической конференции «Старт в медицину» 2021 года
|
Актуальность
В последние годы фторхинолоны всё чаще применяются для лечения туберкулёза. Однако применение данных препаратов сопровождается побочными эффектами, которые можно снизить уменьшением терапевтической дозы лекарства. Наиболее перспективными подходами к решению данной задачи являются микронизация и инкапсулирование лекарственной субстанции в полимерные микрочастицы с использованием сверхкритических флюидных технологий (СКФ).
Одним из ключевых параметров, определяющих эффективность инкапсуляции лекарственного вещества в состав полимерных частиц, является растворимость препарата. Поэтому для разработки метода получения таких частиц с использованием СКФ-технологий необходимо первоначально исследовать влияние условий процесса микронизации на растворимость лекарственной субстанции.
Цель
Изучить влияние условий процесса СКФ-микронизации (состав растворителя и концентрация вещества) на растворимость моксифлоксацина и левофлоксацина.
Задачи
1. Адаптировать метод УФ-спектроскопии для определения растворимости фторхинолонов.
2. Определить оптимальное время растворения препаратов.
3. Провести анализ зависимости скорости растворения микронизированных субстанций левофлоксацина и моксифлоксацина от растворителя и концентрации вещества при микронизации.
Оснащение и оборудование, использованное в работе
• Микроскоп PZOWarsawa
• Магнитная мешалка
• Прибор Ultaspec 2100 American Biosharm
Описание
В качестве объектов исследования были выбраны растворы левофлоксацина и моксифлоксацина в солянокислом буфере (рН=4) и фосфатном буфере (рН=7,5) с концентрацией 1 мг/мл.
Работа состояла из нескольких этапов.
1. Калибровка. Для определения зависимости сигнала от содержания антибиотика в образце были построены калибровочные зависимости.
2. Для определения погрешности метода приготовили растворы моксифлоксацина с известными концентрациями при рН=7,5. Затем измерили оптическую плотность образцов и рассчитали содержание препарата, полученное на практике. Для определения чувствительности метода измерили стандартное отклонение аналитического сигнала фона.
3. Определение оптимального времени растворения препарата. Для этого пробы отбирали через заданные промежутки времени в течение 2 часов, затем определили минимальное время, за которое растворилась большая часть образца. Полного растворения добились с помощью лабораторной мешалки.
4. Определение растворимости. Тест «Растворение» позволяет определить, насколько быстро тот или иной препарат растворится в организме, а также теоретически предсказать, как скоро начнётся его терапевтическое действие. Испытания проводились в условиях, приближенных к физиологическим параметрам, на магнитной мешалке, число оборотов подбирали экспериментально. В качестве среды для растворения использовали растворы, рН которых соответствует показателям рН в разных отделах желудочно-кишечного тракта. Объём среды растворения соответствовал объёму желудка в состоянии натощак + стакан воды (500–900 мл). Температура соответствовала температуре жидкости организма +37 оС и сохранялась в течение всего эксперимента. Для получения отрицательного контроля проводили центрифугирование полученных растворов дважды в течение 15 минут при 13000 об/мин. Через заданные промежутки времени (5, 10, 15 мин) отбирали аликвоты
надосадочной жидкости в 25 мкл, центрифугировали в течение 15 мин при 13000 об/мин. Далее отбирали ещё 15 мкл и повторяли центрифугирование. Методом последовательного разбавления приготовили растворы с концентрациями 0,0025; 0,005; 0,0075 и 0,01 мг/мл. Растворы помещали в кварцевые кюветы и регистрировали УФ-спектры с помощью прибора Ultaspec 2100 AmericanBiosharm в диапазоне длин волн 260–320 нм.
Для поиска наибольшей растворимости использовались микронизированные образцы левофлоксацина и моксифлоксацина, у которых варьировались растворитель и концентрация при микронизации. Микронизированные препараты были получены методом SAS-микронизации. Для этого образцы растворяли в органических растворителях (ДМФА и ДМСО), затем с помощью СК-СО2 растворитель испарялся, и происходило осаждение частиц.
По полученным данным строили градуировочные графики.
5. Микроскопический анализ образцов исследуемых препаратов. Небольшое количество препарата (нативные и микронизированные образцы) помещали на предметное стекло, добавляли каплю буферного раствора и наблюдали изменения под микроскопом PZOWarsawa.
Результаты
1. Оптимизирована методика определения растворимости фторхинолонов, левофлоксацина и моксифлоксацина с применением УФ-спектроскопии.
2. Определено оптимальное время растворения препаратов как в кислой среде (pH=4), имитирующей кислотность желудка, так и в слабощелочной (pH=7,5), что соответствует кислотности кишечника.
3. Согласно полученным результатам в интервале концентраций левофлоксацина и моксифлоксацина 0,0025–0,01 мг/мл (при рН=4 и рН=7,5) сигнал линейно зависит от растворимости. Поэтому в ходе дальнейшего эксперимента концентрации моксифлоксацина и левофлоксацина лежали в экспериментально полученном диапазоне.
4. Для левофлоксацина самая большая разница в растворимостях между нативным и микронизированными образцами наблюдается через 5 мин. Поэтому для дальнейшего исследования выбрали именно эту «точку».
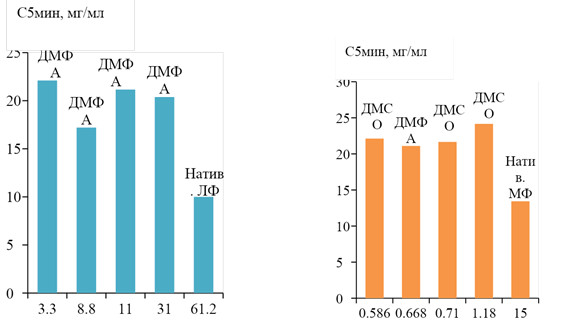
Зависимость растворимости образцов левофлоксацина (слева) и моксифлоксацина (справа) через 5 минут от размеров частиц при рН=4.
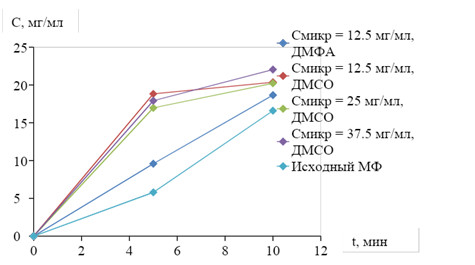
Зависимость растворимости образцов моксифлоксацина от времени растворения при рН = 7,5.
Выводы
1. Дифференцирующее время растворения для образцов фторхинолонов составляет 15 минут.
2. Растворимость микронизированных образцов зависит от условий микронизации: от используемого растворителя и концентрации препарата.
3. Растворимость всех микронизированных образцов исследуемых препаратов выше в 1,5-2 раза по сравнению с исходными образцами веществ.
4. Микронизация методом СКФ с использованием различных растворителей (ДМФА, ДМСО) позволяет получать частицы различной морфологии – от вытянутых игольчатых кристаллов до пластин с неровными краями и размерами от 0,5 до 30 микрон.
Сотрудничество с вузом при создании работы
ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), кафедра химии института фармации им. А.П. Нелюбина