в московской школе
Ферментные цитотоксические препараты для терапии опухолевых заболеваний
|
Работа призёра открытой городской научно-практической конференции «Старт в медицину» в секции «Биохимия» |
Направление работы: Медицина, Биохимия, Биоинженерия
Авторы работы: ГБОУ Школа № 1354 «Вектор»
Email: Написать
Предметы: Биология, Химия
Классы: 10 класс
Мероприятия: Открытая городская научно-практическая конференция «Старт в медицину» 2020 года
|
Актуальность
В современной медицине имеются действенные способы борьбы с опухолевыми заболеваниями, но вопрос метода борьбы с метастазами, который обладал бы высокой эффективностью при минимальном количестве побочных эффектов, остаётся открытым. В настоящее время применяются различные подходы, одним из которых является метод ферментных цитотоксических препаратов. Он заключается в способности нарушать метаболизм аминокислоты аспарагина, которая необходима опухолевым клеткам. L-аспарагиназа является наиболее известным препаратом данной группы; на стадии доклинических испытаний находятся ферментные препараты, показывающие высокую эффективность борьбы с опухолевыми клетками: L-метионин-гамма-лиаза и L-лизин-альфа-оксидаза.
Цель
Определить цитотоксическое действие мутантных форм L-аспарагиназы RrA на клетках линии SkBr-3 карциномы молочной железы человека.
Задачи
1. Изучить причины и механизмы злокачественной трансформации клеток.
2. Изучить современные ферментные препараты для терапии опухолевых заболеваний.
3. Исследовать цитотоксическое действие ферментных препаратов.
4. Оценить полученный результат.
Оснащение и оборудование, использованное в работе
• CO2-инкубатор для культивирования клеток
• Ламинарный шкаф HeraSafe
• Инвертированный микроскоп Biomed-3
• Спектрофотометр Multiscan
• 96-луночный планшет для инкубации клеток с RrA
• Планшетный ридер
• Химическая посуда
• Химические реактивы

Описание
В работе использовали клетки линии SkBr-3 карциномы молочной железы человека из коллекции института биомедицинской химии имени В. Н. Ореховича. Клетки культивировали в среде RPMI-1640, содержащей 10%-ю эмбриональную телячью сыворотку при +37 °C в атмосфере с 5% CO2 и 95% влажности.
Сначала автор приготовил ростовую среду, произвёл посев и культивирование клеток.

Во флакон со средой RPMI-1640 добавили эмбриональную телячью сыворотку до конечной концентрации 10% и получили полную питательную среду. Криопробирку с клеточной линией SkBr-3 достали из криохранилища с жидким азотом. В культуральный флакон добавили 5 мл полной питательной среды. В центрифужную пробирку перенесли содержимое оттаявшей криопробирки и добавили ещё 10 мл полной питательной среды для удаления криопротектора. Центрифугировали 5 мин. при 800 x g, затем слили надосадочную жидкость. Осадок клеток ресуспендировали в 1 мл полной питательной среды, перенесли в культуральный флакон, затем – в СO2-инкубатор (температура +37 °C, 5% CO2, 95% влажности).
Проверка действия ферментного цитотоксического препарата.
Мутантные формы L-аспарагиназ RrA получены методом генетической инженерии в лаборатории ИБМХ. Они отличаются аминокислотами в активном центре фермента RrA и обладают различной ферментативной активностью, т. е. способностью разрушать аспарагин. Для оценки цитотоксической активности использовали МТТ-тест. В его основе лежит принцип восстановления жёлтой соли тетразолия митохондриальными редуктазами (дегидрогеназами) живых клеток до пурпурных кристаллов формазана, которые нерастворимы в водной среде роста клеток. Эта процедура убивает живые клетки, то есть МТТ-тест является конечной точкой исследования. Однако преимуществами данного метода являются экономичность и высокая воспроизводимость результатов.
Посев клеток в 96-луночный планшет. Из флакона CO2-инкубатора удалили питательную среду, для разделения клеток промыли дважды тёплым трипсин-ЭДТА 0,25% объёмом 2 мл и нкубировали при +37 °C в течение 7 мин. Убедившись, что клетки открепились, перенесли их в центрифужную пробирку и центрифугировал 5 мин. при 800 x g. Осадок ресуспендировали в 2 мл полной питательной среды и подсчитывали количество клеток с помощью камеры Горяева в инвертированном микроскопе. Затем автор приготовил суспензию клеток 1x106 клеток в 10 мл полной питательной среды и высеял в планшет в количестве 100 мкл (1x104 клеток на лунку). Клетки культивировали в течение 24-х часов в CO2-инкубаторе.
Далее тестируемые мутантные формы RrA развели фосфатно-солевым буферным раствором до концентрации 1 мг/мл и добавляли 100 мкл к клеткам в каждую лунку
96-луночного планшета. В контрольную лунку добавляли только 100 мкл растворителя (раствор фосфатно-солевого буфера). Инкубировали клетки в течение 48 часов в CO2-инкубаторе.
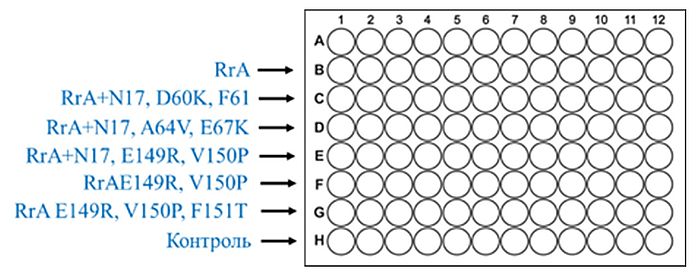
Для приготовления рабочего раствора реактива МТТ взвесили 200 мг МТТ и растворили его в 40 мл тёплого раствора фосфатно-солевого буфера (конечная концентрация 5 мг/мл).
Затем провели МТТ-тест. После инкубации в каждую лунку внесли по 20 мкл готового раствора МТТ и инкубировали 3 часа в CO2-инкубаторе.
Обработку результатов автор провёл следующим образом. В каждой лунке ростовую среду удалили и добавили неполярный растворитель ДМСО для растворения кристаллов формазана.

Оптическую плотность в каждой лунке измеряли на планшетном ридере при длине волны 540 нм. Статистическую обработку результатов провели в программе Excel. Выживаемость клеток в экспериментальных группах оценивали по отношению к контрольной группе. Среднее значение выживаемости оценивали по восьми независимым повторам, учитывая стандартную ошибку отклонения. Достоверными считали результаты при ошибке (р) не более 5%.
Результаты
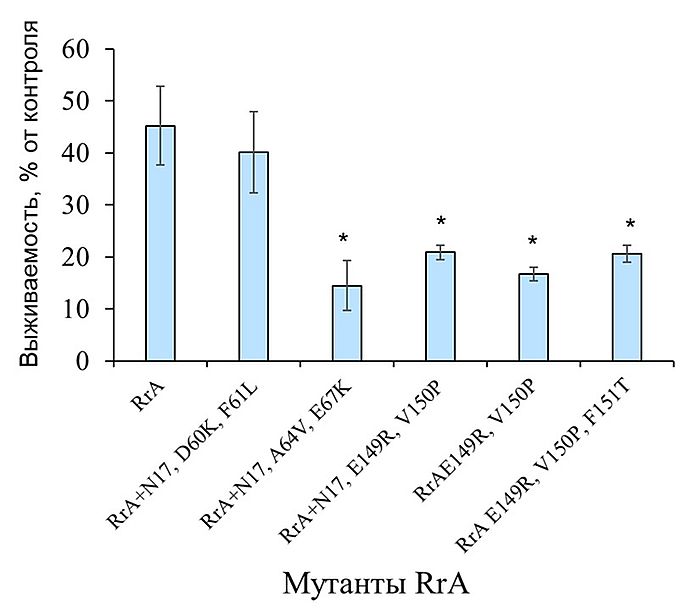
Наибольшей цитотоксической активностью обладали несколько мутантных форм. Выживаемость клеток в этих группах была ниже более чем в два раза по сравнению с группой клеток, обработанных исходной формой RrA. Цитотоксическая активность мутантных форм других образцов хотя и отличалась достоверно от исходной RrA, но была ниже, чем у наиболее активных форм.
Гистограмма выживаемости клеток SkBr-3 (карцинома молочной железы человека) через 48 ч инкубации с мутантными формами RrA
Показаны среднее значение ± стандартное отклонение, статистическая погрешность: * p ≤ 0,05 по отношению к RrA.
Выводы
1. Мутантные формы RrА+N17, A64V, E67K и RrAE149R, V150P обладают наибольшей цитотоксической активностью на клетках SkBr-3.
2. Данные препараты являются наиболее перспективными для создания на их основе противоопухолевого препарата и будут выбраны для дальнейшего изучения.
Перспективы использования результатов работы
Улучшение свойств ферментных препаратов путём генной инженерии приведёт к созданию форм с усиленной цитотоксической активностью по отношению к опухолевым клеткам. На основе данных мутантных форм возможно создание противоопухолевых препаратов.
Сотрудничество с учреждением при создании работы
ФГБНУ «НИИ биомедицинской химии имени В. Н. Ореховича» (ИБМХ)
Награды/достижения
Конкурс для школьников «Юный медик», РУДН – 1 место.
Мнение автора
«При выполнении проекта получены опыт работы в лабораторных условиях и новые знания в области онкологических заболеваний и методов их лечения. Я считаю, что тема очень интересная как для ознакомления, так и для дальнейшего более детального изучения. Проект «Медицинский класс в московской школе» позволяет показать свой потенциал, определиться с будущим направления в медицине, химии и биологии. Он даёт шанс воплотить свои знания в жизни, проведя исследовательскую работу, отработать свои умения. Конференция «Старт в медицину» помогает уже сейчас выбрать дело по душе и показать свои способности. Желаю будущим участникам удачи, терпения, никогда не сдавайтесь и у вас всё получится!»